KR20150093440A - 유기 전계 발광 소자 - Google Patents
유기 전계 발광 소자 Download PDFInfo
- Publication number
- KR20150093440A KR20150093440A KR1020140014216A KR20140014216A KR20150093440A KR 20150093440 A KR20150093440 A KR 20150093440A KR 1020140014216 A KR1020140014216 A KR 1020140014216A KR 20140014216 A KR20140014216 A KR 20140014216A KR 20150093440 A KR20150093440 A KR 20150093440A
- Authority
- KR
- South Korea
- Prior art keywords
- substituted
- unsubstituted
- compound
- organic electroluminescent
- formula
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 claims abstract description 101
- -1 aromatic heterocyclic derivative compound Chemical class 0.000 claims abstract description 36
- 239000002019 doping agent Substances 0.000 claims abstract description 34
- 229910052757 nitrogen Inorganic materials 0.000 claims abstract description 21
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 claims abstract description 11
- 125000003118 aryl group Chemical group 0.000 claims description 42
- 125000004432 carbon atom Chemical group C* 0.000 claims description 21
- 125000001072 heteroaryl group Chemical group 0.000 claims description 19
- 125000000923 (C1-C30) alkyl group Chemical group 0.000 claims description 17
- 229910052760 oxygen Inorganic materials 0.000 claims description 13
- 125000005842 heteroatom Chemical group 0.000 claims description 12
- 229910052717 sulfur Chemical group 0.000 claims description 12
- 229910052736 halogen Inorganic materials 0.000 claims description 11
- 150000002367 halogens Chemical class 0.000 claims description 11
- 229910052799 carbon Inorganic materials 0.000 claims description 10
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 10
- 238000002347 injection Methods 0.000 claims description 10
- 239000007924 injection Substances 0.000 claims description 10
- 125000002950 monocyclic group Chemical group 0.000 claims description 10
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 claims description 9
- 125000002723 alicyclic group Chemical group 0.000 claims description 9
- 229910052783 alkali metal Inorganic materials 0.000 claims description 9
- 150000001340 alkali metals Chemical class 0.000 claims description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical group [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 9
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 claims description 9
- 239000001301 oxygen Chemical group 0.000 claims description 9
- 229910052761 rare earth metal Inorganic materials 0.000 claims description 9
- 150000002910 rare earth metals Chemical class 0.000 claims description 9
- 239000000126 substance Substances 0.000 claims description 9
- 239000011593 sulfur Chemical group 0.000 claims description 9
- 229910052784 alkaline earth metal Inorganic materials 0.000 claims description 8
- 150000001342 alkaline earth metals Chemical class 0.000 claims description 8
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 7
- 229910052805 deuterium Inorganic materials 0.000 claims description 7
- 229910052739 hydrogen Inorganic materials 0.000 claims description 7
- 239000001257 hydrogen Substances 0.000 claims description 7
- 125000001424 substituent group Chemical group 0.000 claims description 6
- 125000000732 arylene group Chemical group 0.000 claims description 5
- 150000004820 halides Chemical class 0.000 claims description 5
- 125000005549 heteroarylene group Chemical group 0.000 claims description 5
- 238000000034 method Methods 0.000 claims description 5
- 150000002894 organic compounds Chemical class 0.000 claims description 5
- 239000000758 substrate Substances 0.000 claims description 4
- 125000002947 alkylene group Chemical group 0.000 claims description 3
- 150000002431 hydrogen Chemical class 0.000 claims 3
- 239000010410 layer Substances 0.000 description 93
- 239000000463 material Substances 0.000 description 38
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 15
- VLKZOEOYAKHREP-UHFFFAOYSA-N hexane Substances CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 15
- 239000007787 solid Substances 0.000 description 14
- 238000004519 manufacturing process Methods 0.000 description 13
- 230000002829 reductive effect Effects 0.000 description 12
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 11
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- 239000000203 mixture Substances 0.000 description 8
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 8
- 238000004020 luminiscence type Methods 0.000 description 7
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 7
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 125000004429 atom Chemical group 0.000 description 6
- 230000000903 blocking effect Effects 0.000 description 6
- 125000000304 alkynyl group Chemical group 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 239000012153 distilled water Substances 0.000 description 5
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 5
- 239000012044 organic layer Substances 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- 125000005104 aryl silyl group Chemical group 0.000 description 4
- 125000000319 biphenyl-4-yl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- ABRVLXLNVJHDRQ-UHFFFAOYSA-N [2-pyridin-3-yl-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound FC(C1=CC(=CC(=N1)C=1C=NC=CC=1)CN)(F)F ABRVLXLNVJHDRQ-UHFFFAOYSA-N 0.000 description 3
- 125000003342 alkenyl group Chemical group 0.000 description 3
- 150000004770 chalcogenides Chemical class 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 239000010408 film Substances 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 3
- 230000005525 hole transport Effects 0.000 description 3
- IMKMFBIYHXBKRX-UHFFFAOYSA-M lithium;quinoline-2-carboxylate Chemical compound [Li+].C1=CC=CC2=NC(C(=O)[O-])=CC=C21 IMKMFBIYHXBKRX-UHFFFAOYSA-M 0.000 description 3
- 229910044991 metal oxide Inorganic materials 0.000 description 3
- 150000004706 metal oxides Chemical class 0.000 description 3
- 150000002739 metals Chemical class 0.000 description 3
- 239000011368 organic material Substances 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- BBMHARZCALWXSL-UHFFFAOYSA-M sodium dihydrogenphosphate monohydrate Chemical compound O.[Na+].OP(O)([O-])=O BBMHARZCALWXSL-UHFFFAOYSA-M 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 3
- 239000010409 thin film Substances 0.000 description 3
- 238000001771 vacuum deposition Methods 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- 0 C*1C(C=C=C2)=C2C(C=CC)=C1C=CO Chemical compound C*1C(C=C=C2)=C2C(C=CC)=C1C=CO 0.000 description 2
- 125000000739 C2-C30 alkenyl group Chemical group 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- ZEEBGORNQSEQBE-UHFFFAOYSA-N [2-(3-phenylphenoxy)-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound C1(=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)C1=CC=CC=C1 ZEEBGORNQSEQBE-UHFFFAOYSA-N 0.000 description 2
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- 238000000151 deposition Methods 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 230000005611 electricity Effects 0.000 description 2
- 230000005281 excited state Effects 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 229910001507 metal halide Inorganic materials 0.000 description 2
- 150000005309 metal halides Chemical class 0.000 description 2
- 230000001590 oxidative effect Effects 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 230000027756 respiratory electron transport chain Effects 0.000 description 2
- 239000002344 surface layer Substances 0.000 description 2
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 150000003624 transition metals Chemical class 0.000 description 2
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 2
- BWHDROKFUHTORW-UHFFFAOYSA-N tritert-butylphosphane Chemical compound CC(C)(C)P(C(C)(C)C)C(C)(C)C BWHDROKFUHTORW-UHFFFAOYSA-N 0.000 description 2
- 238000007738 vacuum evaporation Methods 0.000 description 2
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- 125000004973 1-butenyl group Chemical group C(=CCC)* 0.000 description 1
- 125000004972 1-butynyl group Chemical group [H]C([H])([H])C([H])([H])C#C* 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- 125000000530 1-propynyl group Chemical group [H]C([H])([H])C#C* 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- JUFYHUWBLXKCJM-UHFFFAOYSA-N 2,6-dibromoanthracene-9,10-dione Chemical compound BrC1=CC=C2C(=O)C3=CC(Br)=CC=C3C(=O)C2=C1 JUFYHUWBLXKCJM-UHFFFAOYSA-N 0.000 description 1
- MBHPOBSZPYEADG-UHFFFAOYSA-N 2-bromo-9,9-dimethylfluorene Chemical compound C1=C(Br)C=C2C(C)(C)C3=CC=CC=C3C2=C1 MBHPOBSZPYEADG-UHFFFAOYSA-N 0.000 description 1
- FXSCJZNMWILAJO-UHFFFAOYSA-N 2-bromo-9h-fluorene Chemical compound C1=CC=C2C3=CC=C(Br)C=C3CC2=C1 FXSCJZNMWILAJO-UHFFFAOYSA-N 0.000 description 1
- APSMUYYLXZULMS-UHFFFAOYSA-N 2-bromonaphthalene Chemical compound C1=CC=CC2=CC(Br)=CC=C21 APSMUYYLXZULMS-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- 125000000069 2-butynyl group Chemical group [H]C([H])([H])C#CC([H])([H])* 0.000 description 1
- FPKCTSIVDAWGFA-UHFFFAOYSA-N 2-chloroanthracene-9,10-dione Chemical compound C1=CC=C2C(=O)C3=CC(Cl)=CC=C3C(=O)C2=C1 FPKCTSIVDAWGFA-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000000474 3-butynyl group Chemical group [H]C#CC([H])([H])C([H])([H])* 0.000 description 1
- YOZHUJDVYMRYDM-UHFFFAOYSA-N 4-(4-anilinophenyl)-3-naphthalen-1-yl-n-phenylaniline Chemical compound C=1C=C(C=2C(=CC(NC=3C=CC=CC=3)=CC=2)C=2C3=CC=CC=C3C=CC=2)C=CC=1NC1=CC=CC=C1 YOZHUJDVYMRYDM-UHFFFAOYSA-N 0.000 description 1
- KTERPBUFTWOSJB-UHFFFAOYSA-N 4-naphthalen-1-yl-1-N,1-N-diphenylcyclohexa-1,5-diene-1,4-diamine Chemical compound C1(=CC=CC2=CC=CC=C12)C1(CC=C(C=C1)N(C1=CC=CC=C1)C1=CC=CC=C1)N KTERPBUFTWOSJB-UHFFFAOYSA-N 0.000 description 1
- VIZUPBYFLORCRA-UHFFFAOYSA-N 9,10-dinaphthalen-2-ylanthracene Chemical compound C12=CC=CC=C2C(C2=CC3=CC=CC=C3C=C2)=C(C=CC=C2)C2=C1C1=CC=C(C=CC=C2)C2=C1 VIZUPBYFLORCRA-UHFFFAOYSA-N 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical class [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- 229910004261 CaF 2 Inorganic materials 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 239000002841 Lewis acid Substances 0.000 description 1
- 229910018068 Li 2 O Inorganic materials 0.000 description 1
- 239000004235 Orange GGN Substances 0.000 description 1
- 229910003564 SiAlON Inorganic materials 0.000 description 1
- DHXVGJBLRPWPCS-UHFFFAOYSA-N Tetrahydropyran Chemical compound C1CCOCC1 DHXVGJBLRPWPCS-UHFFFAOYSA-N 0.000 description 1
- XSTXAVWGXDQKEL-UHFFFAOYSA-N Trichloroethylene Chemical group ClC=C(Cl)Cl XSTXAVWGXDQKEL-UHFFFAOYSA-N 0.000 description 1
- 150000001339 alkali metal compounds Chemical class 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000003282 alkyl amino group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 150000001454 anthracenes Chemical class 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 150000004984 aromatic diamines Chemical class 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 125000001769 aryl amino group Chemical group 0.000 description 1
- 125000005129 aryl carbonyl group Chemical group 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 125000002047 benzodioxolyl group Chemical group O1OC(C2=C1C=CC=C2)* 0.000 description 1
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 125000005872 benzooxazolyl group Chemical group 0.000 description 1
- 125000005874 benzothiadiazolyl group Chemical group 0.000 description 1
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- NEUUGXVQQYIMER-UHFFFAOYSA-N c(cc1)ccc1-[n](c1ccccc1c1c2)c1ccc2-c(cc1)ccc1-[n]1c(cc(c(c2ccccc22)c3)[n]2-c2ccccc2)c3c2ccccc12 Chemical compound c(cc1)ccc1-[n](c1ccccc1c1c2)c1ccc2-c(cc1)ccc1-[n]1c(cc(c(c2ccccc22)c3)[n]2-c2ccccc2)c3c2ccccc12 NEUUGXVQQYIMER-UHFFFAOYSA-N 0.000 description 1
- JJOGVVFMVITUQH-UHFFFAOYSA-N c(cc1)ccc1-[n](c1ccccc1c1c2)c1ccc2-c(cc1)ccc1-[n]1c2ccc(c3ccccc3[o]3)c3c2c2c1cccc2 Chemical compound c(cc1)ccc1-[n](c1ccccc1c1c2)c1ccc2-c(cc1)ccc1-[n]1c2ccc(c3ccccc3[o]3)c3c2c2c1cccc2 JJOGVVFMVITUQH-UHFFFAOYSA-N 0.000 description 1
- WIDFXBVKVXCAKW-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1N(c1ccccc1)c(cc1)ccc1-c(cc1)ccc1-[n]1c(cc(c(c2cc(-c3cc(N(c(cc4)ccc4-c4ccccc4)c(cc4)ccc4-c(cc4)ccc4-[n](c4ccccc44)c(cc5)c4c4c5c(cccc5)c5[o]4)ccc3)ccc22)c3)[n]2-c2ccccc2)c3c2ccccc12 Chemical compound c(cc1)ccc1-c(cc1)ccc1N(c1ccccc1)c(cc1)ccc1-c(cc1)ccc1-[n]1c(cc(c(c2cc(-c3cc(N(c(cc4)ccc4-c4ccccc4)c(cc4)ccc4-c(cc4)ccc4-[n](c4ccccc44)c(cc5)c4c4c5c(cccc5)c5[o]4)ccc3)ccc22)c3)[n]2-c2ccccc2)c3c2ccccc12 WIDFXBVKVXCAKW-UHFFFAOYSA-N 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 150000001768 cations Chemical class 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000000392 cycloalkenyl group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000005401 electroluminescence Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 125000003914 fluoranthenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC=C4C1=C23)* 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 229930195733 hydrocarbon Natural products 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- LPAGFVYQRIESJQ-UHFFFAOYSA-N indoline Chemical compound C1=CC=C2NCCC2=C1 LPAGFVYQRIESJQ-UHFFFAOYSA-N 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 238000007733 ion plating Methods 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000000904 isoindolyl group Chemical group C=1(NC=C2C=CC=CC12)* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 125000001786 isothiazolyl group Chemical group 0.000 description 1
- 125000000842 isoxazolyl group Chemical group 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- 150000007517 lewis acids Chemical class 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- ZGEGCLOFRBLKSE-UHFFFAOYSA-N methylene hexane Natural products CCCCCC=C ZGEGCLOFRBLKSE-UHFFFAOYSA-N 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 125000001715 oxadiazolyl group Chemical group 0.000 description 1
- 125000002971 oxazolyl group Chemical group 0.000 description 1
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 1
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- 125000004934 phenanthridinyl group Chemical group C1(=CC=CC2=NC=C3C=CC=CC3=C12)* 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000001725 pyrenyl group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 238000005215 recombination Methods 0.000 description 1
- 230000006798 recombination Effects 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 229910052814 silicon oxide Inorganic materials 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- 238000004544 sputter deposition Methods 0.000 description 1
- 239000004173 sunset yellow FCF Substances 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 125000001935 tetracenyl group Chemical group C1(=CC=CC2=CC3=CC4=CC=CC=C4C=C3C=C12)* 0.000 description 1
- RAOIDOHSFRTOEL-UHFFFAOYSA-N tetrahydrothiophene Chemical compound C1CCSC1 RAOIDOHSFRTOEL-UHFFFAOYSA-N 0.000 description 1
- 125000005247 tetrazinyl group Chemical group N1=NN=NC(=C1)* 0.000 description 1
- 125000003831 tetrazolyl group Chemical group 0.000 description 1
- 238000005979 thermal decomposition reaction Methods 0.000 description 1
- 125000001113 thiadiazolyl group Chemical group 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000001425 triazolyl group Chemical group 0.000 description 1
- 125000003960 triphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)* 0.000 description 1
- NHDIQVFFNDKAQU-UHFFFAOYSA-N tripropan-2-yl borate Chemical compound CC(C)OB(OC(C)C)OC(C)C NHDIQVFFNDKAQU-UHFFFAOYSA-N 0.000 description 1
- 238000004506 ultrasonic cleaning Methods 0.000 description 1
- 238000002061 vacuum sublimation Methods 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Organic Chemistry (AREA)
- Optics & Photonics (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
본 발명은 형광성 그린 호스트 화합물과 도펀트 화합물을 함유하는 발광층을 포함하고, 발광층과 음극(캐소드) 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는 유기 전계 발광 소자에 관한 것으로서, 상기 소자는 구동 전압이 낮고, 발광 효율, 전력 효율 및 수명 특성이 개선된 장점이 있다.
Description
본 발명은 형광성 그린 호스트 화합물과 도펀트 화합물을 함유하는 발광층을 포함하고, 발광층과 음극(캐소드) 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는 유기 전계 발광 소자에 관한 것이다.
전계 발광 소자(electroluminescence device: EL 소자)는 자체 발광형 표시 소자로서 시야각이 넓고 콘트라스트가 우수할 뿐만 아니라 응답속도가 빠르다는 장점을 가지고 있다. 1987년 이스트만 코닥(Eastman Kodak)사는 발광층 형성용 재료로서 저분자인 방향족 다이아민과 알루미늄 착물을 이용하는 유기 EL 소자를 처음으로 개발하였다[참조: Appl. Phys. Lett. 51, 913, 987].
유기 EL 소자는 유기 발광 재료에 전기를 가해 전기 에너지를 빛으로 바꾸는 소자로서, 통상 양극(애노드) 및 음극과 이들 사이에 유기물층을 포함하는 구조를 가진다. 유기 EL 소자의 유기물층은 정공주입층, 정공전달층, 전자차단층, 발광층(호스트 및 도펀트 재료 포함), 전자전달층, 정공차단층, 전자주입층 등으로 이루어질 수 있으며, 유기물층에 사용되는 재료는 기능에 따라 정공주입 재료, 정공전달 재료, 전자차단 재료, 발광 재료, 전자전달 재료, 정공차단 재료, 전자주입 재료 등으로 나뉜다. 이러한 유기 EL 소자에서는 전압 인가에 의해 양극에서 정공이, 음극에서 전자가 발광층에 주입되고, 정공과 전자의 재결합에 의해 에너지가 높은 엑시톤이 형성된다. 이 에너지에 의해 발광 유기 화합물이 여기 상태로 되며, 발광 유기 화합물의 여기 상태가 기저 상태로 돌아가면서 에너지를 빛으로 방출하여 발광하게 된다.
유기 EL 소자의 발광 재료는 소자의 발광 효율을 결정하는 가장 중요한 요인으로서, 발광 재료는 양자 효율이 높고 전자와 정공의 이동도가 커야 하고, 형성된 발광 재료층은 균일하고 안정해야 한다. 이러한 발광 재료는 발광색에 따라 청색, 녹색 또는 적색 발광 재료로 나뉘고, 추가로 노란색 또는 주황색 발광 재료도 있다. 또한, 발광 재료는 기능적인 측면에서 호스트 재료와 도펀트 재료로 구분될 수 있는데 일반적으로 EL 특성이 가장 우수한 소자 구조로는 호스트에 도펀트를 도핑하여 발광층을 만드는 것으로 알려져 있다. 최근에 고효율 및 장수명의 유기 EL 소자의 개발이 시급한 과제로 대두되고 있는데, 특히 중대형 OLED 패널에서 요구하고 있는 EL 특성 수준을 고려해 볼 때 기존의 발광 재료에 비해 매우 우수한 재료의 개발이 시급한 실정이다. 이를 위하여 고체 상태의 용매 및 에너지 전달자 역할을 하는 호스트 물질의 바람직한 특성은 순도가 높아야 하며, 진공증착이 가능하도록 적당한 분자량을 가져야 한다. 또한 유리 전이온도와 열분해온도가 높아 열적 안정성을 확보해야 하며, 장수명화를 위해 높은 전기화학적 안정성이 요구되며, 무정형 박막을 형성하기 용이해야 하며, 인접한 다른 층의 재료들과는 접착력이 좋은 반면 층간 이동은 하지 않아야 한다.
발광 재료는 색순도, 발광 효율 및 안정성을 향상시키기 위해 호스트와 도펀트를 혼합하여 사용할 수 있다. 일반적으로, EL 특성이 우수한 소자는 호스트에 도펀트를 도핑하여 만들어진 발광층을 포함하는 구조이다. 이와 같은 도펀트/호스트 재료 체계를 사용할 때, 호스트 재료는 발광 소자의 효율과 성능에 큰 영향을 미치므로, 그 선택이 중요하다.
기존의 도펀트 화합물과 호스트 화합물을 함유하는 발광 재료를 유기 전계 발광 소자에 적용하는 경우, 전력 효율이 좋지 못하고 작동 수명 측면에서도 만족스럽지 못하여 발광 효율 면에서 문제점을 나타내었다.
대한민국 공개특허공보 제10-2010-0002153호, 제10-2009-0093897호, 제10-2011-0019940호 및 제10-2011-0027033호는 정공주입층, 정공전달층, 전자차단층, 발광층, 전자전달층, 정공차단층, 전자주입층 등에 사용될 수 있는 안트라센 유도체 또는 아민 유도체를 포함하는 유기 전계 발광 소자를 기재하고 있으나, 특정한 조합의 호스트 화합물과 도펀트 화합물을 발광층에 포함하고, 발광층과 음극 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는 유기 전계 발광 소자에 대하여 언급하고 있지 않다.
본 발명자들은 특정 조합의 호스트 화합물 및 도펀트 화합물을 발광층에 함유하고, 발광층과 음극 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는 유기 전계 발광 소자가 개선된 전력 효율, 발광 효율 및 수명 특성을 제공함을 밝혀내고 본 발명을 완성하게 되었다.
따라서, 본 발명의 목적은 구동 전압이 낮고, 발광 효율, 전력 효율 및 수명 특성이 개선된 유기 전계 발광 소자를 제공하는 것이다.
상기의 목적을 달성하기 위하여, 본 발명은 하기 화학식 1로 표시되는 호스트 화합물과 하기 화학식 2로 표시되는 도펀트 화합물을 함유한 발광층을 포함하고, 상기 발광층과 음극 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는 유기 전계 발광 소자를 제공한다.
[화학식 1]
상기 화학식 1에서,
Ar1 및 Ar2는 각각 독립적으로 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고,
Ar3은 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이다.
[화학식 2]
상기 화학식 2에서,
Ar4 및 Ar5는 각각 독립적으로 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고,
A 고리 및 B 고리는 각각 독립적으로 하기 구조에서 선택되며.
R1 내지 R7은 각각 독립적으로 수소, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C1-C30)알콕시, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (3-30원)헤테로아릴이거나, 인접한 치환기끼리 결합하여 치환 또는 비치환된 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있고, 상기 형성된 지환족 또는 방향족 환의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있다.
본 발명에 따르면 구동 전압이 낮고, 발광 효율, 전력 효율 및 수명 특성이 개선된 유기 전계 발광 소자를 제공할 수 있다.
이하에서 본 발명을 더욱 상세히 설명하나, 이는 설명을 위한 것으로 본 발명의 범위를 제한하는 방법으로 해석되어서는 안된다.
본 발명은 상기 화학식 1로 표시되는 호스트 화합물과 상기 화학식 2로 표시되는 도펀트 화합물이 함유된 발광층을 포함하고, 발광층과 음극 사이에, 예를 들면, 전자전달층, 전자주입층, 또는 이들 둘 다에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는 유기 전계 발광 소자에 관한 것이다.
상기 질소 함유 방향족 헤테로시클릭 유도체 화합물은 하기 화학식 3으로 표시될 수 있다.
[화학식 3]
상기 화학식 3에서,
HAr은 하기 화학식에서 선택되며,
L은 단일결합, 치환 또는 비치환된 (C6-C30)아릴렌, 또는 치환 또는 비치환된 (5-30원)헤테로아릴렌이고,
R13은 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이며,
R14 내지 R26은 각각 독립적으로 수소, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C1-C30)알콕시, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이거나, 인접한 치환기끼리 결합하여 치환 또는 비치환된 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있고, 상기 형성된 지환족 또는 방향족 환의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있으며,
a는 0 내지 3의 정수이고, a가 2 이상의 정수일 때 각각의 R13은 동일하거나 상이할 수 있으며,
b는 1 또는 2이고, b가 2일 때 각각의 (-L-HAr)은 동일하거나 상이할 수 있다.
추가로, 상기 질소 함유 방향족 헤테로시클릭 유도체 화합물은 하기 화학식 4로 표시될 수 있다.
[화학식 4]
상기 화학식 4에서,
X1 및 X2는 각각 독립적으로 CR12 또는 N이고,
L1 및 L2는 각각 독립적으로 단일결합, 치환 또는 비치환된 (C1-C30)알킬렌, 치환 또는 비치환된 (C6-C30)아릴렌, 또는 치환 또는 비치환된 (3-30원)헤테로아릴렌이며;
R11 및 R12는 각각 독립적으로 수소, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C1-C30)알콕시, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (3-30원)헤테로아릴이거나, 인접한 R11과 R12는 서로 융합하여 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있으며, 상기 형성된 지환족 또는 방향족 고리의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있고;
c는 1 내지 3의 정수이고, c가 2 이상의 정수일 때 각각의 (-L1-L2-R11)은 동일하거나 상이할 수 있다.
본원에 기재되어 있는 "(C1-C30)알킬(렌)"은 탄소수가 1 내지 30개인 직쇄 또는 분지쇄 알킬(렌)을 의미하고, 여기에서 탄소수가 1 내지 20개인 것이 바람직하고, 1 내지 10개인 것이 더 바람직하다. 상기 알킬의 구체적인 예로서, 메틸, 에틸, n-프로필, 이소프로필, n-부틸, 이소부틸 및 3급-부틸 등이 있다. 본원에서 "(C2-C30)알케닐"은 탄소수가 2 내지 30개인 직쇄 또는 분지쇄 알케닐을 의미하고, 여기에서 탄소수가 2 내지 20개인 것이 바람직하고, 2 내지 10개인 것이 더 바람직하다. 상기 알케닐의 구체적인 예로서, 비닐, 1-프로페닐, 2-프로페닐, 1-부테닐, 2-부테닐, 3-부테닐, 2-메틸부트-2-에닐 등이 있다. 본원에서 "(C2-C30)알키닐"은 탄소수가 2 내지 30개인 직쇄 또는 분지쇄 알키닐을 의미하고, 여기에서 탄소수가 2 내지 20개인 것이 바람직하고, 2 내지 10개인 것이 더 바람직하다. 상기 알키닐의 예로서, 에티닐, 1-프로피닐, 2-프로피닐, 1-부티닐, 2-부티닐, 3-부티닐, 1-메틸펜트-2-이닐 등이 있다. 본원에서 "(C3-C30)시클로알킬"은 탄소수가 3 내지 30개인 단일환 또는 다환 탄화수소를 의미하고, 여기에서 탄소수가 3 내지 20개인 것이 바람직하고, 3 내지 7개인 것이 더 바람직하다. 상기 시클로알킬의 예로서, 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실 등이 있다. 본원에서 "(3-7원)헤테로시클로알킬"은 환 골격 원자수가 3 내지 7개, 바람직하게는 5 내지 7개이고, B, N, O, S, P(=O), Si 및 P로 이루어진 군에서 선택된 하나 이상의 헤테로원자, 바람직하게는 O, S 및 N에서 선택되는 하나 이상의 헤테로원자를 포함하는 시클로알킬을 의미하고, 예를 들어, 테트라히드로푸란, 피롤리딘, 티올란, 테트라히드로피란 등이 있다. 본원에서 "(C6-C30)아릴(렌)"은 탄소수가 6 내지 30개인 방향족 탄화수소에서 유래된 단일환 또는 융합환계 라디칼을 의미하고, 여기에서 환 골격 탄소수가 6 내지 20개인 것이 바람직하고, 6 내지 15개인 것이 더 바람직하다. 상기 아릴의 예로서, 페닐, 바이페닐, 터페닐, 나프틸, 플루오레닐, 페난트레닐, 안트라세닐, 인데닐, 트리페닐레닐, 피레닐, 테트라세닐, 페릴레닐, 크라이세닐, 나프타세닐, 플루오란테닐 등이 있다. 본원에서 "(3-30원)헤테로아릴(렌)"은 환 골격 원자수가 3 내지 30개이고, B, N, O, S, P(=O), Si 및 P로 이루어진 군에서 선택된 하나 이상의 헤테로원자를 포함하는 아릴기를 의미한다. 여기에서 환 골격 원자수가 3 내지 20개인 것이 바람직하고, 3 내지 15개인 것이 더 바람직하다. 헤테로원자수는 바람직하게는 1 내지 4개이고, 단일 환계이거나 하나 이상의 벤젠환과 축합된 융합환계일 수 있으며, 부분적으로 포화될 수도 있다. 또한, 본원에서 상기 헤테로아릴(렌)은 하나 이상의 헤테로아릴 또는 아릴기가 단일 결합에 의해 헤테로아릴기와 연결된 형태도 포함한다. 상기 헤테로아릴의 예로서, 푸릴, 티오펜일, 피롤릴, 이미다졸릴, 피라졸릴, 티아졸릴, 티아디아졸릴, 이소티아졸릴, 이속사졸릴, 옥사졸릴, 옥사디아졸릴, 트리아진일, 테트라진일, 트리아졸릴, 테트라졸릴, 푸라잔일, 피리딜, 피라진일, 피리미딘일, 피리다진일 등의 단일 환계 헤테로아릴, 벤조푸란일, 벤조티오펜일, 이소벤조푸란일, 디벤조푸란일, 디벤조티오펜일, 벤조이미다졸릴, 벤조티아졸릴, 벤조이소티아졸릴, 벤조이속사졸릴, 벤조옥사졸릴, 이소인돌릴, 인돌릴, 인다졸릴, 벤조티아디아졸릴, 퀴놀릴, 이소퀴놀릴, 신놀리닐, 퀴나졸리닐, 퀴녹살리닐, 카바졸릴, 페녹사진일, 페난트리딘일, 벤조디옥솔릴 등의 융합 환계 헤테로아릴 등이 있다. 본원에서 "할로겐"은 F, Cl, Br 및 I 원자를 포함한다.
또한, 본원에 기재되어 있는 "치환 또는 비치환"이라는 기재에서 "치환"은 어떤 작용기에서 수소 원자가 다른 원자 또는 다른 작용기(즉, 치환체)로 대체되는 것을 뜻한다. 본 발명의 상기 화학식들에서 치환 (C1-C30)알킬, 치환 (C1-C30)알콕시, 치환 (C3-C30)시클로알킬, 치환 (C6-C30)아릴(렌), 치환 (3-30원)헤테로아릴(렌), 및 치환 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리의 치환체는 각각 독립적으로, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, (C1-C30)알킬, 할로(C1-C30)알킬, (C2-C30)알케닐, (C2-C30)알키닐, (C1-C30)알콕시, (C1-C30)알킬티오, (C3-C30)시클로알킬, (C3-C30)시클로알케닐, (3-7원)헤테로시클로알킬, (C6-C30)아릴옥시, (C6-C30)아릴티오, (C6-C30)아릴로 치환되거나 비치환된 (3-30원)헤테로아릴, (3-30원)헤테로아릴로 치환되거나 비치환된 (C6-C30)아릴, 트리(C1-C30)알킬실릴, 트리(C6-C30)아릴실릴, 디(C1-C30)알킬(C6-C30)아릴실릴, (C1-C30)알킬디(C6-C30)아릴실릴, 아미노, 모노 또는 디(C1-C30)알킬아미노, 모노 또는 디(C6-C30)아릴아미노, (C1-C30)알킬(C6-C30)아릴아미노, (C1-C30)알킬카보닐, (C1-C30)알콕시카보닐, (C6-C30)아릴카보닐, 디(C6-C30)아릴보로닐, 디(C1-C30)알킬보로닐, (C1-C30)알킬(C6-C30)아릴보로닐, (C6-C30)아르(C1-C30)알킬 및 (C1-C30)알킬(C6-C30)아릴로 이루어진 군으로부터 선택되는 1종 이상의 것이다.
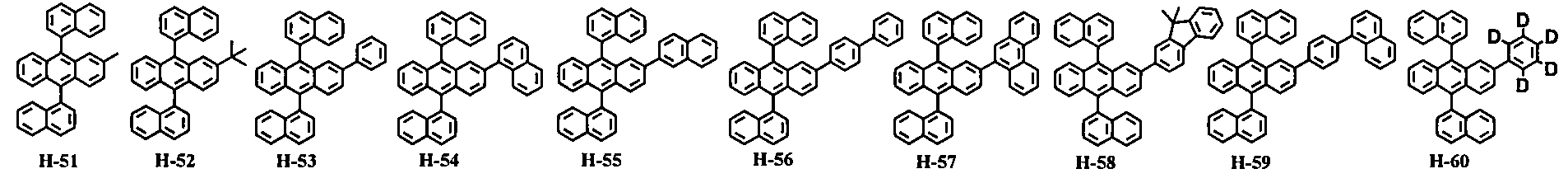
상기 화학식 1로 표시되는 화합물은 하기 화합물로 이루어진 군으로부터 선택되나, 이에 제한되는 것은 아니다.
상기 화학식 2로 표시되는 화합물은 하기 화합물로 이루어진 군으로부터 선택되나, 이에 제한되는 것은 아니다.
상기 화학식 3으로 표시되는 화합물은 하기 화합물로 이루어진 군으로부터 선택되나, 이에 제한되는 것은 아니다.
상기 화학식 4로 표시되는 화합물은 하기 화합물로 이루어진 군으로부터 선택되나, 이에 제한되는 것은 아니다.
본 발명에 따른 유기 전계 발광 소자는 제1 전극; 제2 전극; 및 상기 제1 전극 및 제2 전극 사이에 개재되는 1층 이상의 유기물층을 가지며, 상기 유기물층은 발광층을 포함하고, 상기 발광층은 상기 화학식 1로 표시되는 호스트 화합물 및 상기 화학식 2로 표시되는 도펀트 화합물을 포함한다. 상기 발광층의 의미는 발광이 이루어지는 층으로서 단일층일 수 있으며, 또한 2개 이상의 층이 적층된 복수의 층일 수 있다. 상기 발광층의 호스트 화합물에 대한 도펀트 화합물의 도핑 농도가 20중량% 미만인 것이 바람직하다.
또한, 본 발명에 따른 유기 전계 발광 소자는 상기 발광층과 음극 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는데, 이 화합물은 유기물층에 포함되는 전자전달층, 전자주입층, 또는 이들 둘 다에 사용될 수 있다. 상기 전자전달층, 전자주입층, 또는 이들 둘 다는 환원성 도펀트를 함유할 수 있고, 상기 환원성 도펀트는 알칼리 금속, 알칼리 토류 금속, 희토류 금속, 알칼리 금속의 산화물, 알칼리 금속의 할로젠화물, 알칼리 토류 금속의 산화물, 알칼리 토류 금속의 할로젠화물, 희토류 금속의 산화물, 희토류 금속의 할로젠화물, 알칼리 금속의 유기 착체, 알칼리 토류 금속의 유기 착체 및 희토류 금속의 유기 착체로 이루어진 군으로부터 선택되는 1종 이상의 것이다.
본 발명의 다른 양태에 의하면, 본 발명은 상기 화학식 1로 표시되는 호스트 화합물 및 상기 화학식 2로 표시되는 도펀트 화합물의 호스트/도펀트 조합을 제공하며, 이러한 호스트/도펀트 조합을 포함하는 유기 전계 발광 소자를 제공한다.
본 발명의 또 다른 양태에 의하면, 본 발명은 상기 화학식 1로 표시되는 호스트 화합물 및 상기 화학식 2로 표시되는 도펀트 화합물을 포함하는 발광층과 양극 사이에 버퍼층을 추가로 포함할 수 있다.
상기 버퍼층 재료는 하기 화학식 5 내지 화학식 8로 표시되는 화합물로 구성된 군으로부터 선택될 수 있다
[화학식 5]
[화학식 6]
[화학식 7]
[화학식 8]
M1-Cz-L4-Cz-M2
Cz는 하기 구조이며,
상기 화학식 5 내지 8에서
X는 -CR101- 또는 -N-이고;
Y1 및 Y2는 각각 독립적으로 -O-, -S-, -N(R109)-, -C(R110)(R111)-이고, Y1과 Y2가 동시에 존재하는 경우는 없으며;
L3 및 L4는 각각 독립적으로 단일결합, 치환 또는 비치환된 (C6-C30)아릴렌, 또는 치환 또는 비치환된 (5-30원)헤테로아릴렌이고;
Ar1, Ar2, Ar3, M1 및 M2는 각각 독립적으로 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고, Ar1과 Ar2는 융합하여 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있으며, 상기 형성된 지환족 또는 방향족 고리의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있고;
R101 내지 R108은 각각 독립적으로 수소, 중수소, 할로겐, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 치환 또는 비치환된 (3-30원)헤테로아릴 또는 -SiR112R113R114이고, 두 개의 인접한 R102는 융합하여 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있으며, 상기 형성된 지환족 또는 방향족 고리의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있고, R107과 M1 또는 M2는 융합하여 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있고, 상기 형성된 지환족 또는 방향족 고리의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있고, L3과 R101이 각각 페닐인 경우는 융합하여 플루오렌이 형성될 수 있으며;
R109 내지 R111은 각각 독립적으로 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고, R109 및 R111은 서로 동일하거나 상이할 수 있으며;
R112 내지 R114는 각각 독립적으로 치환 또는 비치환된 (C1-C30)알킬, 또는 치환 또는 비치환된 (C6-C30)아릴이며;
h는 1 또는 2의 정수이고;
i, j, k 및 q는 각각 독립적으로 1 내지 4의 정수이며;
p는 1 내지 3의 정수이고;
h, p 및 q가 2 이상의 정수인 경우 각각의 치환기는 동일하거나 상이할 수 있다.
상기 버퍼층 재료는 하기 화합물로 이루어진 군으로부터 선택되나, 이에 제한되는 것은 아니다.
본 발명에 따른 호스트 화합물 및 도펀트 화합물은 당업자에게 공지된 합성 방법으로 제조할 수 있으며, 예를 들면 하기 반응식 1 및 2에 따라 제조할 수 있다.
1) 호스트 반응식 1
상기 반응식 1에서 Ar1, Ar2 및 Ar3은 화학식 1에서의 정의와 동일하고, Hal은 할로겐이다.
2) 도펀트 반응식 2
상기 반응식 2에서 Ar4, Ar5, A 고리 및 B 고리는 화학식 2에서의 정의와 동일하고, Hal은 할로겐이다.
본 발명의 유기 전계 발광 소자는 유기물층에 아릴아민계 화합물 및 스티릴아릴아민계 화합물로 이루어진 군으로부터 선택된 하나 이상의 화합물을 추가로 포함할 수도 있다.
또한, 본 발명의 유기 전계 발광 소자에 있어서, 유기물층은 1족, 2족, 4주기 전이금속, 5주기 전이금속, 란탄 계열 금속 및 d-전이원소의 유기 금속으로 이루어진 군으로부터 선택되는 하나 이상의 금속, 또는 이러한 금속을 포함하는 하나 이상의 착체 화합물을 추가로 포함할 수도 있다.
본 발명의 유기 전계 발광 소자에 있어서, 한 쌍의 전극의 적어도 한 쪽의 내측 표면에, 칼코제나이드(chalcogenide)층, 할로겐화 금속층 및 금속 산화물층으로부터 선택되는 하나 이상의 층(이하, 이들을 "표면층"이라고 지칭함)을 배치하는 것이 바람직하다. 구체적으로는, 발광 매체층 측의 양극 표면에 규소 및 알루미늄의 칼코제나이드(산화물을 포함한다)층을, 또한 발광 매체층 측의 음극 표면에 할로겐화 금속층 또는 금속 산화물층을 배치하는 것이 바람직하다. 상기 표면층에 의해 유기 전계 발광 소자의 구동 안정화를 얻을 수 있다. 상기 칼코제나이드의 바람직한 예로는 SiOX(1≤X≤2), AlOX(1≤X≤1.5), SiON 또는 SiAlON 등이 있고, 할로겐화 금속의 바람직한 예로는 LiF, MgF2, CaF2, 불화 희토류 금속 등이 있으며, 금속 산화물의 바람직한 예로는 Cs2O, Li2O, MgO, SrO, BaO, CaO 등이 있다.
또한, 본 발명의 유기 전계 발광 소자에 있어서, 한 쌍의 전극의 적어도 한 쪽의 표면에 전자 전달 화합물과 환원성 도펀트의 혼합 영역, 또는 정공 전달 화합물과 산화성 도펀트의 혼합 영역을 배치하는 것도 바람직하다. 이러한 방식에 의해 전자 전달 화합물이 음이온으로 환원되므로 혼합 영역으로부터 발광 매체에 전자를 주입 및 전달하기 용이해진다. 또한, 정공 전달 화합물은 산화되어 양이온으로 되므로 혼합 영역으로부터 발광 매체에 정공을 주입 및 전달하기 용이해진다. 바람직한 산화성 도펀트로서는 각종 루이스산 및 억셉터(acceptor) 화합물을 들 수 있고, 바람직한 환원성 도펀트로는 알칼리 금속, 알칼리 금속 화합물, 알칼리 토류 금속, 희토류 금속 및 이들의 혼합물을 들 수 있다. 또한 환원성 도펀트층을 전하생성층으로 사용하여 두 개 이상의 발광층을 가진, 백색 발광을 하는 유기 전계 발광 소자를 제작할 수 있다.
본 발명의 유기 전계 발광 소자의 각 층의 형성은 진공증착, 스퍼터링, 플라즈마, 이온플레이팅 등의 건식 성막법이나, 스핀코팅, 침지 코팅(dip coating), 플로우 코팅 등의 습식 성막법 중 어느 하나의 방법을 적용할 수 있다.
습식 성막법의 경우, 각 층을 형성하는 재료를 에탄올, 클로로포름, 테트라하이드로푸란, 디옥산 등의 적절한 용매에 용해 또는 분산시켜 박막을 형성하는데, 그 용매는 각 층을 형성하는 재료가 용해 또는 분산될 수 있고, 성막성에 문제가 없는 것이라면 어느 것이어도 된다.
이하에서, 본 발명의 상세한 이해를 위하여 본 발명의 호스트 화합물 및 도펀트 화합물의 제조방법을 설명한다.
[실시예 1] 화합물 H-33의 제조
화합물 1-1의 제조
2-브로모나프탈렌(819g, 3.96mol)에 테트라하이드로퓨란(THF)(5L)을 넣고 실온에서 10분 동안 교반하여 완전히 녹이고 -72℃로 온도를 낮춘 후, n-부틸리튬(1.6M, n-헥산 중)(2.68L, 4.285mol)을 천천히 적가하였다. 1시간 뒤, 2-클로로안트라퀴논(400g, 1.648mol)을 가한 후, 천천히 실온으로 온도를 올리며 26시간 동안 교반하였다. 포화된 암모늄클로라이드 용액을 가해 1시간 동안 교반한 후 감압 여과하였다. 유기층을 분리하여 증발시켜 갈색 고체인 화합물 1-1(551g, 67%)을 얻었다.
화합물 1-2의 제조
화합물 1-1(551g, 1.104mol), 칼륨아이오다이드(733g, 4.42mol), 나트륨포스페이트모노하이드레이트(NaH2PO2·H2O)(937g, 8.8mol) 및 아세트산(3.35L, 0.33M)을 넣고 환류 교반하였다. 21시간 후 실온으로 냉각시킨 후 감압 여과하였다. 감압 여과 후 얻은 고체에 소량의 칼륨 카보네이트와 증류수를 가해 중성으로 만들고, 2시간 동안 교반한 후 유기층을 분리하여 증발시켜 연두빛 고체인 화합물 1-2(318g, 62%)를 얻었다.
화합물 1-3의 제조
화합물 1-2(318g, 0.68mol) 및 테트라히드로퓨란(2.3L)을 넣고 실온에서 10분 동안 교반하여 완전히 녹이고 -72℃로 온도를 낮춘 후, n-부틸리튬(1.6M, n-헥산 중)(0.56L, 0.89mol)을 천천히 적가하였다. 1시간 뒤, 트리아이소프로필보레이트(206g, 1.09mol)를 가한 후, 천천히 실온으로 온도를 올리며 24시간 동안 교반하였다. 10% HCl 용액 2L를 가해 2시간 동안 교반한 후 감압 여과하였다. 유기층을 분리하여 증발시키고 헥산과 메탄올을 이용하여 재결정하여 살구색 고체인 화합물 1-3(188g, 58%)을 얻었다.
화합물 H-33의 제조
화합물 1-3(11g, 23.19mmol), 2-브로모-9,9-다이메틸-9H-플루오렌(7.6g, 27.83mmol), 트란스-디클로로비스트리페닐포스핀 팔라듐(II)(0.326g, 0.464mmol), 나트륨카보네이트(5.41g, 51.02mmol), 톨루엔(100mL) 및 증류수(10mL)를 넣고 환류 교반하였다. 30시간 뒤 실온으로 온도를 낮춘 뒤 증류수 100mL를 가해 반응을 종료시켰다. 이때 생기는 고체를 감압 여과하였다. 얻어진 고체를 헥산과 메탄올을 이용하여 재결정하여 노란색 고체인 화합물 H-33(8.52g, 61%)을 얻었다.
[실시예 2] 화합물 D-7의 제조
화합물 2-1의 제조
2-브로모플루오렌 74g(270.7mmol)을 건조된 테트라하이드로퓨란 용매 500mL에 녹인 후에, -78℃에서 2.5M n-부틸리튬(n-butyllithium, 2.5M, 헥산 중) 130.0mL(324.9mmol)를 천천히 적가하였다. 1시간 동안 교반한 후에 2,6-디브로모안트라센-9,10-디온(2,7-dichloroanthracene-9,10-dione) 30.0g(108.3mmol)을 첨가하고 천천히 실온으로 올리면서 교반하였다. 17시간 뒤 물을 넣고 30분 동안 교반하고 에틸 아세테이트(EA) 500mL로 추출하고 물 500mL로 세척한 후 얻은 유기층에 황산마그네슘을 넣어 수분을 제거한 후 감압 증류하고 건조시켜 화합물 2-1, 150.8g(200mmol)을 얻었다.
화합물 2-2의 제조
화합물 2-1, 11g(14.51mmol), 칼륨아이오다이드(KI) 9.64g(58.06mmol), 나트륨포스페이트모노하이드레이트 9.24g(87.12mmol)을 아세트산 150mL에 녹이고 환류 교반하였다. 14시간 후 25℃로 냉각시킨 후 수산화나트륨 200mL를 넣어 중화한 후에, 물 400mL로 씻어준 후 다이클로로메탄 용매 300mL로 추출하고, 황산마그네슘으로 건조시키고, 필터 여과하여 용매를 감압 제거한 후에 얻어진 화합물을 메틸렌 클로라이드/헥산 = 1/100 조건 하에서 컬럼 분리하여 화합물 2-2, 5.4g(7.5mmol)을 얻었다.
화합물 D-7의 제조
화합물 2-2, 4.9g(6.79mmol), 인돌린 2.1g(16.99mmol), 팔라듐(II) 아세테이트[Pd(OAc)2] 0.07g(0.33mmol), 트리-t-부틸포스핀[P(t-Bu)3](50%, 톨루엔 중) 0.3mL(0.67mmol), Cs2CO3 6.6g(20.38mmol) 및 톨루엔 50mL를 넣고 110℃에서 5시간 동안 교반하였다. 메탄올을 50mL 넣고 생성된 고체를 감압 여과하였다. 고체를 증류수, 메탄올 및 헥산으로 씻어 주었다. 고체를 EA 100mL와 섞고 2시간 동안 환류 교반하였다. 감압 여과 후 고체를 컬럼 분리하였다. 얻어진 고체를 THF에 녹이고 메탄올을 넣어서 생성된 고체를 감압 여과하여 화합물 D-7, 2.6g(3.3mmol)을 얻었다.
[소자 실시예 1] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
본 발명의 발광 재료를 이용한 구조의 OLED 소자를 제작하였다. 우선, OLED용 글래스(삼성-코닝사 제조)로부터 얻어진 투명 전극 ITO 박막(15Ω/□)을, 트리클로로에틸렌, 아세톤, 에탄올 및 증류수를 순차적으로 사용하여 초음파 세척을 실시한 후, 이소프로판올에 넣어 보관한 후 사용하였다. 다음으로 진공 증착 장비의 기판 홀더에 ITO 기판을 장착한 후, 진공 증착장비 내의 셀에 N1,N1'-([1,1'-바이페닐]-4,4'-디일)비스(N1-(나프탈렌-1-일)-N4,N4-디페닐벤젠-1,4-디아민)을 넣고 챔버 내의 진공도가 10-6torr에 도달할 때까지 배기시킨 후, 셀에 전류를 인가하여 증발시켜 ITO 기판 위에 60nm 두께의 정공주입층을 증착하였다. 이어서, 진공 증착 장비 내의 다른 셀에 N1,N1'-디(나프탈렌-1-일)-N4,N4'-디페닐바이페닐-4,4'-디아민을 넣고, 셀에 전류를 인가하여 증발시켜 정공주입층 위에 20nm 두께의 정공전달층을 증착하였다. 진공 증착 장비 내의 한쪽 셀에 호스트로서 화합물 H-33을 넣고, 또 다른 셀에는 도펀트로서 화합물 D-7을 넣은 후, 두 물질을 다른 속도로 증발시켜 호스트와 도펀트의 합계량에 대해 도펀트를 2중량%의 양으로 도핑함으로써 상기 정공전달층 위에 35nm 두께의 발광층을 증착하였다. 이어서, 상기 발광층 위에 전자전달층으로서 한쪽 셀에 화합물 E-2를 넣고, 또 다른 셀에는 리튬 퀴놀레이트를 넣은 후, 두 물질을 같은 속도로 증발시켜 각각 50중량%의 양으로 도핑함으로써 20nm 두께의 전자전달층을 증착하였다. 이어서 전자주입층으로 리튬 퀴놀레이트를 2nm 두께로 증착한 후, 다른 진공 증착 장비를 이용하여 Al 음극을 150nm의 두께로 증착하여 OLED 소자를 제작하였다. 재료 별로 각 화합물은 10-6torr 하에서 진공 승화 정제하여 사용하였다.
그 결과, 3.4V의 전압에서 3.9mA/cm2의 전류가 흘렀으며, 1000cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 20시간 이상이었다.
[소자 실시예 2] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
전자전달층으로서 화합물 E-2 대신 화합물 E-112를 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.3V의 전압에서 4.0mA/cm2의 전류가 흘렀으며, 1050cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 22시간 이상이었다.
[소자 실시예 3] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
전자전달층으로서 화합물 E-2 대신 화합물 E-89를 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.2V의 전압에서 4.8mA/cm2의 전류가 흘렀으며, 1100cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 18시간 이상이었다.
[소자 실시예 4] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
전자전달층으로서 화합물 E-2 대신 화합물 E-56을 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.1V의 전압에서 3.8mA/cm2의 전류가 흘렀으며, 900cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 22시간 이상이었다.
[소자 실시예 5] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
전자전달층으로서 화합물 E-2 대신 화합물 E-111을 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.2V의 전압에서 3.9mA/cm2의 전류가 흘렀으며, 1040cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 23시간 이상이었다.
[소자 실시예 6] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
전자전달층으로서 화합물 E-2 대신 화합물 E-110을 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.1V의 전압에서 3.8mA/cm2의 전류가 흘렀으며, 980cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 22시간 이상이었다.
[소자 실시예 7] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
전자전달층으로서 화합물 E-2 대신 화합물 E-42를 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.1V의 전압에서 4.3mA/cm2의 전류가 흘렀으며, 950cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 22시간 이상이었다.
[소자 실시예 8] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
정공주입층과 발광층 사이에 N,N'-디(4-바이페닐)-N,N'-디(4-바이페닐)-4,4'-디아미노바이페닐을 넣고, 셀에 전류를 인가하여 증발시켜 10nm 두께의 정공전달층을 증착한 후, 화합물 B-18을 10nm 두께로 증착한 다음 발광층을 증착한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.5V의 전압에서 3.3mA/cm2의 전류가 흘렀으며, 1000cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 17시간 이상이었다.
[소자 실시예 9] 본 발명에 따른 유기 전계 발광 화합물을 이용한 OLED 소자 제작
정공주입층과 발광층 사이에 N,N'-디(4-바이페닐)-N,N'-디(4-바이페닐)-4,4'-디아미노바이페닐을 넣고, 셀에 전류를 인가하여 증발시켜 10nm 두께의 정공전달층을 증착한 후, 화합물 B-2를 10nm 두께로 증착한 다음 발광층을 증착하고, 전자전달층으로서 한쪽 셀에 화합물 E-2 대신 E-112를 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.6V의 전압에서 3.5mA/cm2의 전류가 흘렀으며, 1070cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 20시간 이상이었다.
[비교예 1] 종래의 발광 재료를 이용한 OLED 소자 제작
전자전달층으로서 한쪽 셀에 화합물 E-2를 넣고, 또 다른 셀에는 리튬 퀴놀레이트를 넣은 후, 두 물질을 같은 속도로 증발시켜 각각 50중량%의 양으로 도핑함으로써 20nm 두께의 전자전달층을 증착한 것 대신 Alq3를 증착한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 5.2V의 전압에서 5.3mA/cm2의 전류가 흘렀으며, 1000cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 10시간 이상이었다.
[비교예 2] 종래의 발광 재료를 이용한 OLED 소자 제작
발광 재료로서 도펀트에 화합물 D-5를 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.5V의 전압에서 4.6mA/cm2의 전류가 흘렀으며, 1000cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 15시간 이상이었다.
[비교예 3] 종래의 발광 재료를 이용한 OLED 소자 제작
발광 재료로서 호스트에 화합물 ADN(9,10-디(나프탈렌-2-일)안트라센)을 사용한 것 외에는 소자 실시예 1과 동일한 방법으로 OLED 소자를 제작하였다.
그 결과, 3.4V의 전압에서 4.5mA/cm2의 전류가 흘렀으며, 1000cd/m2의 녹색 발광이 확인되었고, 15000nit의 휘도에서 발광이 90%로 떨어지는데 걸린 시간이 15시간 이상이었다.
본 발명의 유기 전계 발광 소자는 특정 도펀트 화합물과 호스트 화합물의 조합을 함유하는 발광층을 포함하고, 발광층과 음극 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함함으로써, 종래의 발광 재료를 이용한 소자보다 소자의 전류 특성을 개선시킴으로써, 소자의 구동전압을 낮추고 동시에 전류효율 및 전력효율이 향상된 OLED 소자를 제조할 수 있는 장점이 있으며, 수명도 향상되는 장점이 있다.
Claims (11)
- 기판상에 양극 및 음극으로 이루어진 한 쌍의 전극과 그 전극 사이에 발광층을 가지며, 그 발광층은 하기 화학식 1로 표시되는 호스트 및 하기 화학식 2로 표시되는 도펀트를 포함하고, 상기 발광층과 음극 사이에 질소 함유 방향족 헤테로시클릭 유도체 화합물을 포함하는, 유기 전계 발광 소자.
[화학식 1]
상기 화학식 1에서,
Ar1 및 Ar2는 각각 독립적으로 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고,
Ar3은 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이다.
[화학식 2]
상기 화학식 2에서,
Ar4 및 Ar5는 각각 독립적으로 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이고,
A 고리 및 B 고리는 각각 독립적으로 하기 구조에서 선택되며.
R1 내지 R7은 각각 독립적으로 수소, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C1-C30)알콕시, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (3-30원)헤테로아릴이거나, 인접한 치환기끼리 결합하여 치환 또는 비치환된 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있고, 상기 형성된 지환족 또는 방향족 환의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있다. - 제1항에 있어서, 질소 함유 방향족 헤테로시클릭 유도체 화합물이 하기 화학식 3으로 표시되는, 유기 전계 발광 소자.
[화학식 3]
상기 화학식 3에서,
HAr은 하기 화학식에서 선택되며,
L은 단일결합, 치환 또는 비치환된 (C6-C30)아릴렌, 또는 치환 또는 비치환된 (5-30원)헤테로아릴렌이고,
R13은 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이며,
R14 내지 R26은 각각 독립적으로 수소, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C1-C30)알콕시, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (5-30원)헤테로아릴이거나, 인접한 치환기끼리 결합하여 치환 또는 비치환된 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있고, 상기 형성된 지환족 또는 방향족 환의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있으며,
a는 0 내지 3의 정수이고, a가 2 이상의 정수일 때 각각의 R13은 동일하거나 상이할 수 있으며,
b는 1 또는 2이고, b가 2일 때 각각의 (-L-HAr)은 동일하거나 상이할 수 있다. - 제1항에 있어서, 질소 함유 방향족 헤테로시클릭 유도체 화합물이 하기 화학식 4로 표시되는, 유기 전계 발광 소자.
[화학식 4]
상기 화학식 4에서,
X1 및 X2는 각각 독립적으로 CR12 또는 N이고;
L1 및 L2는 각각 독립적으로 단일결합, 치환 또는 비치환된 (C1-C30)알킬렌, 치환 또는 비치환된 (C6-C30)아릴렌, 또는 치환 또는 비치환된 (3-30원)헤테로아릴렌이며;
R11 및 R12는 각각 독립적으로 수소, 중수소, 할로겐, 시아노, 카르복실, 니트로, 히드록시, 치환 또는 비치환된 (C1-C30)알킬, 치환 또는 비치환된 (C1-C30)알콕시, 치환 또는 비치환된 (C3-C30)시클로알킬, 치환 또는 비치환된 (C6-C30)아릴, 또는 치환 또는 비치환된 (3-30원)헤테로아릴이거나, 인접한 R11과 R12는 서로 융합하여 (C3-C30) 단일환 또는 다환의 지환족 또는 방향족 고리를 형성할 수 있으며, 상기 형성된 지환족 또는 방향족 고리의 탄소 원자는 질소, 산소 및 황으로부터 선택되는 하나 이상의 헤테로원자로 대체될 수 있고;
c는 1 내지 3의 정수이고, c가 2 이상의 정수일 때 각각의 (-L1-L2-R11)은 동일하거나 상이할 수 있다. - 제1항에 있어서, 질소 함유 방향족 헤테로시클릭 유도체 화합물이 전자전달층, 전자주입층, 또는 이들 둘 다에 사용된, 유기 전계 발광 소자.
- 제1항에 있어서, 양극과 발광층 사이에 버퍼층을 추가로 갖는, 유기 전계 발광 소자.
- 제8항에 있어서, 상기 전자전달층, 전자주입층, 또는 이들 둘 다에 환원성 도펀트가 함유된, 유기 전계 발광 소자.
- 제10항에 있어서, 상기 환원성 도펀트가, 알칼리 금속, 알칼리 토류 금속, 희토류 금속, 알칼리 금속의 산화물, 알칼리 금속의 할로젠화물, 알칼리 토류 금속의 산화물, 알칼리 토류 금속의 할로젠화물, 희토류 금속의 산화물, 희토류 금속의 할로젠화물, 알칼리 금속의 유기 착체, 알칼리 토류 금속의 유기 착체 및 희토류 금속의 유기 착체로 이루어진 군으로부터 선택되는 1종 이상의 것인, 유기 전계 발광 소자.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020140014216A KR20150093440A (ko) | 2014-02-07 | 2014-02-07 | 유기 전계 발광 소자 |
| CN201410344388.7A CN104835921A (zh) | 2014-02-07 | 2014-07-18 | 有机电致发光器件 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020140014216A KR20150093440A (ko) | 2014-02-07 | 2014-02-07 | 유기 전계 발광 소자 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150093440A true KR20150093440A (ko) | 2015-08-18 |
Family
ID=53813659
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020140014216A KR20150093440A (ko) | 2014-02-07 | 2014-02-07 | 유기 전계 발광 소자 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR20150093440A (ko) |
| CN (1) | CN104835921A (ko) |
Cited By (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017065415A1 (ko) * | 2015-10-13 | 2017-04-20 | 에스에프씨 주식회사 | 저계조 영역에서의 휘도감소율이 개선된 유기 발광 소자 |
| WO2017151535A1 (en) * | 2016-03-04 | 2017-09-08 | Solvay Usa Inc. | Spirobifluorene derivatives and their use in electron injection layers of organic electronic devices |
| WO2017151537A1 (en) * | 2016-03-04 | 2017-09-08 | Solvay Usa Inc. | Spirobifluorene derivatives and their use in electron transport layers of organic electronic devices |
| WO2017188679A1 (ko) * | 2016-04-28 | 2017-11-02 | 주식회사 엘지화학 | 유기 발광 소자 |
| JP2019503078A (ja) * | 2016-04-28 | 2019-01-31 | エルジー・ケム・リミテッド | 有機発光素子 |
| WO2020009519A1 (ko) * | 2018-07-05 | 2020-01-09 | 주식회사 엘지화학 | 다환 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020022768A1 (ko) * | 2018-07-24 | 2020-01-30 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2020036441A1 (ko) * | 2018-08-14 | 2020-02-20 | 주식회사 엘지화학 | 유기발광소자 |
| CN113678274A (zh) * | 2019-11-11 | 2021-11-19 | 株式会社Lg化学 | 有机发光器件 |
| WO2024196084A1 (ko) * | 2023-03-17 | 2024-09-26 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
Families Citing this family (26)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104592124B (zh) * | 2015-01-04 | 2018-01-02 | 华南理工大学 | 一种萘[1,2]并咪唑双极性共轭化合物及制备与应用 |
| JP2018517289A (ja) * | 2015-05-29 | 2018-06-28 | ダウ グローバル テクノロジーズ エルエルシー | 有機組成物及び該組成物を含む有機層を備える電子デバイス |
| KR102579752B1 (ko) | 2015-12-22 | 2023-09-19 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR20170075122A (ko) * | 2015-12-22 | 2017-07-03 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| KR20170075114A (ko) | 2015-12-22 | 2017-07-03 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| CN107188859A (zh) * | 2016-03-15 | 2017-09-22 | 上海和辉光电有限公司 | 一种有机电致发光化合物及含该化合物的oled器件 |
| EP3436452B1 (en) * | 2016-03-15 | 2023-09-13 | Dow Global Technologies Llc | Organic electroluminescent compound and organic electroluminescent device thereof |
| TWI619703B (zh) * | 2016-05-18 | 2018-04-01 | 昱鐳光電科技股份有限公司 | 用於有機電激發光元件之化合物及使用該化合物之有機電激發光元件 |
| CN106220571A (zh) * | 2016-07-28 | 2016-12-14 | 长春海谱润斯科技有限公司 | 一种含氮杂环衍生物及其在有机电致发光器件中的应用 |
| CN108352449B (zh) * | 2016-10-18 | 2019-10-01 | 株式会社Lg化学 | 有机发光器件 |
| US20200095226A1 (en) * | 2016-12-08 | 2020-03-26 | Guangzhou Chinaray Optoelectronic Materials Ltd. | Triazine fused ring derivative and application thereof in organic electronic device |
| US11158813B2 (en) * | 2017-03-15 | 2021-10-26 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
| US11555018B2 (en) | 2017-12-14 | 2023-01-17 | Jiangsu Sunera Technology Co., Ltd. | Organic compound based on triazine and benzoxazole and application thereof in organic electroluminescent device |
| CN109206420B (zh) * | 2017-12-14 | 2022-08-02 | 江苏三月科技股份有限公司 | 一种基于三嗪的有机化合物及其在有机电致发光器件上的应用 |
| WO2020100946A1 (ja) * | 2018-11-16 | 2020-05-22 | 出光興産株式会社 | 新規化合物、有機エレクトロルミネッセンス素子及び電子機器 |
| CN109608402B (zh) * | 2018-12-29 | 2020-10-02 | 浙江工业大学 | 一种咪唑类衍生物离子化化合物及其制备方法 |
| KR20210125891A (ko) | 2019-02-14 | 2021-10-19 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 호스트 재료용 안트라센 화합물, 발광 디바이스, 발광 장치, 전자 기기, 및 조명 장치 |
| KR20200101838A (ko) * | 2019-02-20 | 2020-08-28 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20210020358A (ko) | 2019-08-14 | 2021-02-24 | 엘지디스플레이 주식회사 | 유기 화합물과 이를 포함하는 유기발광다이오드 및 유기발광표시장치 |
| CN110845422A (zh) * | 2019-11-28 | 2020-02-28 | 吉林奥来德光电材料股份有限公司 | 一种有机发光化合物、其合成方法及有机电致发光器件 |
| CN111087387B (zh) * | 2019-12-26 | 2022-04-29 | 厦门天马微电子有限公司 | 一种有机化合物、显示面板及显示装置 |
| CN112552137A (zh) * | 2020-12-09 | 2021-03-26 | 黑龙江省科学院石油化学研究院 | 一种有机电致发光中间体材料及其合成方法 |
| CN115974805A (zh) * | 2021-10-12 | 2023-04-18 | 烟台显华化工科技有限公司 | 一种蒽类化合物 |
| CN113831292A (zh) * | 2021-10-13 | 2021-12-24 | 上海传勤新材料有限公司 | 一种含有苯并咪唑和蒽的有机电子传输材料及其应用 |
| CN118475576A (zh) * | 2022-01-13 | 2024-08-09 | 保土谷化学工业株式会社 | 嘧啶化合物和有机电致发光元件 |
| CN115286581B (zh) * | 2022-08-02 | 2024-03-22 | 吉林大学 | 具有高固态发光效率的纯有机单分子白光材料及其在制备有机电致白光器件中的应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100696505B1 (ko) * | 2005-03-31 | 2007-03-19 | 삼성에스디아이 주식회사 | 유기 전계 발광 소자 및 그 제조방법 |
| KR101161289B1 (ko) * | 2008-02-29 | 2012-07-02 | 에스에프씨 주식회사 | 아민 유도체 및 이를 채용한 유기전계발광소자 |
| EP2256176A1 (en) * | 2008-06-25 | 2010-12-01 | Gracel Display Inc. | Novel organic electroluminescent compounds and organic electroluminescent device using the same |
| JP2010165977A (ja) * | 2009-01-19 | 2010-07-29 | Sony Corp | 有機電界発光素子、表示装置、および電子機器 |
| DE102009031021A1 (de) * | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| KR101226700B1 (ko) * | 2009-08-21 | 2013-01-25 | 에스에프씨 주식회사 | 아민 유도체 및 이를 채용한 유기전계발광소자 |
-
2014
- 2014-02-07 KR KR1020140014216A patent/KR20150093440A/ko not_active Application Discontinuation
- 2014-07-18 CN CN201410344388.7A patent/CN104835921A/zh active Pending
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017065415A1 (ko) * | 2015-10-13 | 2017-04-20 | 에스에프씨 주식회사 | 저계조 영역에서의 휘도감소율이 개선된 유기 발광 소자 |
| WO2017151535A1 (en) * | 2016-03-04 | 2017-09-08 | Solvay Usa Inc. | Spirobifluorene derivatives and their use in electron injection layers of organic electronic devices |
| WO2017151537A1 (en) * | 2016-03-04 | 2017-09-08 | Solvay Usa Inc. | Spirobifluorene derivatives and their use in electron transport layers of organic electronic devices |
| US11723268B2 (en) | 2016-04-28 | 2023-08-08 | Lg Chem, Ltd. | Organic light-emitting element |
| WO2017188679A1 (ko) * | 2016-04-28 | 2017-11-02 | 주식회사 엘지화학 | 유기 발광 소자 |
| KR20170123062A (ko) * | 2016-04-28 | 2017-11-07 | 주식회사 엘지화학 | 유기 발광 소자 |
| JP2019503078A (ja) * | 2016-04-28 | 2019-01-31 | エルジー・ケム・リミテッド | 有機発光素子 |
| JP2019505091A (ja) * | 2016-04-28 | 2019-02-21 | エルジー・ケム・リミテッド | 有機発光素子 |
| US12082498B2 (en) * | 2016-04-28 | 2024-09-03 | Lg Chem, Ltd. | Organic light-emitting element |
| WO2020009519A1 (ko) * | 2018-07-05 | 2020-01-09 | 주식회사 엘지화학 | 다환 화합물 및 이를 포함하는 유기 발광 소자 |
| WO2020022768A1 (ko) * | 2018-07-24 | 2020-01-30 | 주식회사 엘지화학 | 유기 발광 소자 |
| WO2020036441A1 (ko) * | 2018-08-14 | 2020-02-20 | 주식회사 엘지화학 | 유기발광소자 |
| CN113678274A (zh) * | 2019-11-11 | 2021-11-19 | 株式会社Lg化学 | 有机发光器件 |
| CN113678274B (zh) * | 2019-11-11 | 2023-09-12 | 株式会社Lg化学 | 有机发光器件 |
| CN113678274B9 (zh) * | 2019-11-11 | 2023-10-24 | 株式会社Lg化学 | 有机发光器件 |
| WO2024196084A1 (ko) * | 2023-03-17 | 2024-09-26 | 주식회사 엘지화학 | 화합물 및 이를 포함하는 유기 발광 소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN104835921A (zh) | 2015-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20150093440A (ko) | 유기 전계 발광 소자 | |
| KR101939552B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102128702B1 (ko) | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102157998B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR101429035B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR102182270B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| JP6525382B2 (ja) | 新規な有機電界発光化合物及びそれを含む有機電界発光デバイス | |
| KR102160902B1 (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| US20140061609A1 (en) | Novel compounds for organic electronic material and organic electroluminescent device using the same | |
| KR20150076129A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20140049186A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20140141933A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| US20140346406A1 (en) | Organic electroluminescent device comprising the organic electroluminescent compounds | |
| KR20120038060A (ko) | 신규한 유기 전자재료용 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20150010016A (ko) | 유기 전계 발광 소자 | |
| KR20150128590A (ko) | 전자전달재료 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20150077513A (ko) | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| TW201420582A (zh) | 新穎有機電場發光化合物及含該化合物之有機電場發光裝置 | |
| KR20140125576A (ko) | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20140049181A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| TW201326359A (zh) | 新穎有機電場發光化合物及使用該化合物之有機電場發光裝置 | |
| KR101427620B1 (ko) | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR20150135125A (ko) | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| JP5830097B2 (ja) | 有機電子材料のための新規化合物、およびこれを使用する有機電界発光素子 | |
| KR20140082486A (ko) | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |