KR101290011B1 - 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 - Google Patents
유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 Download PDFInfo
- Publication number
- KR101290011B1 KR101290011B1 KR1020090134613A KR20090134613A KR101290011B1 KR 101290011 B1 KR101290011 B1 KR 101290011B1 KR 1020090134613 A KR1020090134613 A KR 1020090134613A KR 20090134613 A KR20090134613 A KR 20090134613A KR 101290011 B1 KR101290011 B1 KR 101290011B1
- Authority
- KR
- South Korea
- Prior art keywords
- substituted
- unsubstituted
- compound
- aryl
- alkyl
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 83
- 239000000463 material Substances 0.000 claims abstract description 51
- 238000002347 injection Methods 0.000 claims abstract description 24
- 239000007924 injection Substances 0.000 claims abstract description 24
- 239000010410 layer Substances 0.000 claims description 45
- 125000003118 aryl group Chemical group 0.000 claims description 41
- 125000004429 atom Chemical group 0.000 claims description 40
- 125000000217 alkyl group Chemical group 0.000 claims description 28
- 125000001072 heteroaryl group Chemical group 0.000 claims description 25
- 239000012044 organic layer Substances 0.000 claims description 23
- 125000003342 alkenyl group Chemical group 0.000 claims description 20
- 125000003545 alkoxy group Chemical group 0.000 claims description 20
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 20
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 claims description 15
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 14
- 230000005525 hole transport Effects 0.000 claims description 14
- 229910052805 deuterium Inorganic materials 0.000 claims description 13
- 238000000034 method Methods 0.000 claims description 12
- 229910052739 hydrogen Inorganic materials 0.000 claims description 10
- 239000001257 hydrogen Substances 0.000 claims description 10
- 125000000304 alkynyl group Chemical group 0.000 claims description 9
- 125000004104 aryloxy group Chemical group 0.000 claims description 9
- 125000001424 substituent group Chemical group 0.000 claims description 9
- 150000002431 hydrogen Chemical class 0.000 claims description 8
- 125000003282 alkyl amino group Chemical group 0.000 claims description 7
- 125000000732 arylene group Chemical group 0.000 claims description 5
- 125000005549 heteroarylene group Chemical group 0.000 claims description 5
- 125000002950 monocyclic group Chemical group 0.000 claims description 5
- 125000001769 aryl amino group Chemical group 0.000 claims description 4
- 125000004986 diarylamino group Chemical group 0.000 claims description 4
- 125000004585 polycyclic heterocycle group Chemical group 0.000 claims description 4
- 125000001931 aliphatic group Chemical group 0.000 claims description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 2
- 238000004020 luminiscence type Methods 0.000 abstract 1
- 230000015572 biosynthetic process Effects 0.000 description 27
- 238000003786 synthesis reaction Methods 0.000 description 27
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- -1 2-tetrahydrofuranyl Chemical group 0.000 description 13
- 238000006243 chemical reaction Methods 0.000 description 10
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 9
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 9
- 239000012153 distilled water Substances 0.000 description 9
- 239000007787 solid Substances 0.000 description 9
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 9
- 239000002019 doping agent Substances 0.000 description 8
- 239000002904 solvent Substances 0.000 description 7
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 6
- 238000003756 stirring Methods 0.000 description 5
- 239000000758 substrate Substances 0.000 description 5
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 229910052736 halogen Inorganic materials 0.000 description 4
- 150000002367 halogens Chemical class 0.000 description 4
- 125000000623 heterocyclic group Chemical group 0.000 description 4
- 125000005647 linker group Chemical group 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 4
- 150000002825 nitriles Chemical class 0.000 description 4
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 4
- 229910052760 oxygen Inorganic materials 0.000 description 4
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- 239000000243 solution Substances 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical compound C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 125000005842 heteroatom Chemical group 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000004065 semiconductor Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 3
- QENGPZGAWFQWCZ-UHFFFAOYSA-N 3-Methylthiophene Chemical compound CC=1C=CSC=1 QENGPZGAWFQWCZ-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical group C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- AMGQUBHHOARCQH-UHFFFAOYSA-N indium;oxotin Chemical compound [In].[Sn]=O AMGQUBHHOARCQH-UHFFFAOYSA-N 0.000 description 2
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 125000006574 non-aromatic ring group Chemical group 0.000 description 2
- 239000002985 plastic film Substances 0.000 description 2
- NHDIQVFFNDKAQU-UHFFFAOYSA-N tripropan-2-yl borate Chemical compound CC(C)OB(OC(C)C)OC(C)C NHDIQVFFNDKAQU-UHFFFAOYSA-N 0.000 description 2
- 238000001771 vacuum deposition Methods 0.000 description 2
- 239000011787 zinc oxide Substances 0.000 description 2
- YIWGJFPJRAEKMK-UHFFFAOYSA-N 1-(2H-benzotriazol-5-yl)-3-methyl-8-[2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carbonyl]-1,3,8-triazaspiro[4.5]decane-2,4-dione Chemical compound CN1C(=O)N(c2ccc3n[nH]nc3c2)C2(CCN(CC2)C(=O)c2cnc(NCc3cccc(OC(F)(F)F)c3)nc2)C1=O YIWGJFPJRAEKMK-UHFFFAOYSA-N 0.000 description 1
- VEPOHXYIFQMVHW-XOZOLZJESA-N 2,3-dihydroxybutanedioic acid (2S,3S)-3,4-dimethyl-2-phenylmorpholine Chemical compound OC(C(O)C(O)=O)C(O)=O.C[C@H]1[C@@H](OCCN1C)c1ccccc1 VEPOHXYIFQMVHW-XOZOLZJESA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- BWGRDBSNKQABCB-UHFFFAOYSA-N 4,4-difluoro-N-[3-[3-(3-methyl-5-propan-2-yl-1,2,4-triazol-4-yl)-8-azabicyclo[3.2.1]octan-8-yl]-1-thiophen-2-ylpropyl]cyclohexane-1-carboxamide Chemical compound CC(C)C1=NN=C(C)N1C1CC2CCC(C1)N2CCC(NC(=O)C1CCC(F)(F)CC1)C1=CC=CS1 BWGRDBSNKQABCB-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 229910052688 Gadolinium Inorganic materials 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 1
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- 229910006404 SnO 2 Inorganic materials 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- SLGBZMMZGDRARJ-UHFFFAOYSA-N Triphenylene Natural products C1=CC=C2C3=CC=CC=C3C3=CC=CC=C3C2=C1 SLGBZMMZGDRARJ-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 239000012790 adhesive layer Substances 0.000 description 1
- 125000004653 anthracenylene group Chemical group 0.000 description 1
- 125000003710 aryl alkyl group Chemical group 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 229920001940 conductive polymer Polymers 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 238000003618 dip coating Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 125000005567 fluorenylene group Chemical group 0.000 description 1
- UIWYJDYFSGRHKR-UHFFFAOYSA-N gadolinium atom Chemical compound [Gd] UIWYJDYFSGRHKR-UHFFFAOYSA-N 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 150000002390 heteroarenes Chemical class 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- 229910052738 indium Inorganic materials 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 229910003437 indium oxide Inorganic materials 0.000 description 1
- PJXISJQVUVHSOJ-UHFFFAOYSA-N indium(iii) oxide Chemical compound [O-2].[O-2].[O-2].[In+3].[In+3] PJXISJQVUVHSOJ-UHFFFAOYSA-N 0.000 description 1
- 125000003406 indolizinyl group Chemical group C=1(C=CN2C=CC=CC12)* 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 238000007641 inkjet printing Methods 0.000 description 1
- 239000011133 lead Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 239000000203 mixture Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 125000004312 morpholin-2-yl group Chemical group [H]N1C([H])([H])C([H])([H])OC([H])(*)C1([H])[H] 0.000 description 1
- 125000004572 morpholin-3-yl group Chemical group N1C(COCC1)* 0.000 description 1
- 125000004957 naphthylene group Chemical group 0.000 description 1
- 239000007773 negative electrode material Substances 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 125000005562 phenanthrylene group Chemical group 0.000 description 1
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 229920006255 plastic film Polymers 0.000 description 1
- 229920000767 polyaniline Polymers 0.000 description 1
- 229920000128 polypyrrole Polymers 0.000 description 1
- 229920000123 polythiophene Polymers 0.000 description 1
- 239000007774 positive electrode material Substances 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 1
- 125000003373 pyrazinyl group Chemical group 0.000 description 1
- 125000005548 pyrenylene group Chemical group 0.000 description 1
- 125000002098 pyridazinyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N silicon dioxide Inorganic materials O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 238000004528 spin coating Methods 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 238000010345 tape casting Methods 0.000 description 1
- 125000006836 terphenylene group Chemical group 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 239000011135 tin Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 125000004306 triazinyl group Chemical group 0.000 description 1
- 125000005580 triphenylene group Chemical group 0.000 description 1
- 229910052720 vanadium Inorganic materials 0.000 description 1
- GPPXJZIENCGNKB-UHFFFAOYSA-N vanadium Chemical compound [V]#[V] GPPXJZIENCGNKB-UHFFFAOYSA-N 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
- VWQVUPCCIRVNHF-UHFFFAOYSA-N yttrium atom Chemical compound [Y] VWQVUPCCIRVNHF-UHFFFAOYSA-N 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- YVTHLONGBIQYBO-UHFFFAOYSA-N zinc indium(3+) oxygen(2-) Chemical compound [O--].[Zn++].[In+3] YVTHLONGBIQYBO-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
Landscapes
- Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Organic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
Description
본 발명은 전자 수송능, 정공 주입 및/또는 수송능, 및/또는 발광능이 우수한 유기발광 화합물 및 이를 하나 이상의 유기층에 포함함으로써 발광효율, 휘도, 열적 안정성, 구동 전압, 수명 등의 특성이 향상된 유기 전계 발광 소자에 관한 것이다.
유기 전자 소자는 유기 반도체 물질을 이용한 전자 소자로서, 전극과 유기 반도체 물질 사이에서의 정공 및/또는 전자의 교류를 필요로 한다.
유기 전자 소자는 동작 원리에 따라 하기와 같이 크게 두 가지로 나눌 수 있다. 첫째는 외부의 광원으로부터 소자로 유입된 광자에 의하여 유기층에서 엑시톤(exiton)이 형성되고, 이 엑시톤이 전자와 정공으로 분리되고, 이 전자와 정공이 각각 다른 전극으로 전달되어 전류원(전압원)으로 사용되는 형태의 전자 소자이다. 둘째는 2개 이상의 전극에 전압 또는 전류를 가하여 전극과 계면을 이루는 유기 반도체 물질층에 정공 및/또는 전자를 주입하고, 주입된 전자와 정공에 의하여 작동 하는 형태의 전자 소자이다.
유기 전자 소자의 예로는 유기 전계발광(electroluminescent, EL) 소자(이하, 간단히 '유기 EL 소자'로 칭함), 유기 태양 전지, 유기 감광체(OPC) 드럼, 유기 트랜지스터 등이 있으며, 이들은 모두 소자의 구동을 위하여 전자/정공 주입 물질, 전자/정공 추출 물질, 전자/정공 수송 물질 또는 발광 물질을 필요로 한다. 이하에서는 주로 유기 EL 소자에 대하여 구체적으로 설명하지만, 상기 유기 전자 소자들에서는 전자/정공 주입 물질, 전자/정공 추출 물질, 전자/정공 수송 물질 또는 발광 물질이 모두 유사한 원리로 작용한다.
일반적으로 유기 발광 현상이란 유기 물질을 이용하여 전기 에너지를 빛 에너지로 전환시켜 주는 현상을 말한다. 유기 발광 현상을 이용하는 유기 EL 소자는 통상 양극과 음극, 이들 사이에 유기층을 포함하는 구조를 가진다. 여기서 유기층은 유기 EL 소자의 효율과 안정성을 높이기 위하여 각기 다른 물질로 구성된 다층의 구조로 이루어진 경우가 많으며, 예컨대 정공 주입층, 정공 수송층, 발광층, 전자 수송층, 전자 주입층 등을 포함할 수 있다.
이러한 유기 EL 소자의 구조에서 두 전극 사이에 전압을 걸어주게 되면 양극(anode)에서는 정공이, 음극(cathode)에서는 전자가 유기층으로 주입되고, 주입된 정공과 전자가 만났을 때 엑시톤(exciton)이 형성되며, 이 엑시톤이 바닥상태로 떨어질 때 빛이 나게 된다.
유기 EL 소자에서 유기층으로 사용되는 재료는 기능에 따라, 발광 재료와 전하 수송 재료, 정공 주입 재료, 정공 수송 재료, 전자 수송 재료, 전자 주입 재료 등으로 분류될 수 있다.
발광 재료는 발광색에 따라 청색, 녹색, 적색 발광 재료와, 보다 나은 천연색을 구현하기 위해 필요한 노란색 및 주황색 발광 재료로 구분될 수 있다. 또한, 색순도의 증가와 에너지 전이를 통한 발광 효율을 증가시키기 위하여, 발광 재료로서 호스트/도판트 계를 사용할 수 있다. 그 원리는 발광층을 주로 구성하는 호스트보다 에너지 대역 간극이 작고 발광 효율이 우수한 도판트를 발광층에 소량 혼합하면, 호스트에서 발생한 엑시톤이 도판트로 수송되어 효율이 높은 빛을 내는 것이다. 이때 호스트의 파장이 도판트의 파장대로 이동하므로, 이용하는 도판트의 종류에 따라 원하는 파장의 빛을 얻을 수 있다.
특히 인광인 경우 형광에 비해 이론적으로 100%의 발광 효과를 기대할 수 있다. 이로 인해 형광에서의 25%의 발광효율 보다 높은 발광 효율을 가질 수 있다.
그러나 현재 인광 재료의 경우 형광에 비해 개발 속도도 느리고 시제품에 적용시키기에는 수명이 열세가 되고 있다.
유기 EL 소자가 갖는 우수한 특징들을 충분히 발휘하기 위해서는 소자내 유기층을 이루는 물질, 즉 정공 주입 물질, 정공 수송 물질, 발광 물질, 전자 수송 물질, 전자 주입 물질 등이 안정하고 효율적인 재료에 의하여 뒷받침되는 것이 선행되어야 하나, 아직까지 안정하고 효율적인 유기 EL 소자용 유기층 재료의 개발이 충분히 이루어지지 않은 상태이며, 이에 새로운 재료의 개발이 계속 요구되고 있다.
따라서, 본 발명의 목적은 우수한 전자 수송능, 정공 주입 및/또는 수송능 및/또는 발광능(형광 또는 인광)을 가진 유기발광 화합물 및 이를 하나 이상의 유기층에 포함함으로써 발광효율, 휘도, 열적 안정성, 구동 전압, 수명 등의 특성이 향상된 유기 EL 소자를 제공하는 것이다.
상기 목적을 달성하기 위하여 본 발명은 양극; 음극; 및 상기 양극과 음극 사이에 개재(介在)된 하나 이상의 유기층을 포함하는 유기 EL 소자로서, 상기 유기층 중 적어도 하나는 하기 화학식 1의 화합물을 포함하는 것을 특징으로 하는 유기 EL 소자를 제공한다:
<화학식 1>
상기 식에서,
X는 N이고;
A는 치환 또는 비치환된, 핵원자수 6 내지 40의, 모노사이클릭 (monocyclic) 또는 축합 폴리사이클릭(fused polycyclic) 헤테로환(heterocycle)을 의미하되, 적 어도 X-함유 고리는 핵원자수 6 내지 8의 방향족 고리이며;
R1 내지 R10은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며, R5 및 R6은 연결되어 축합고리를 형성할 수 있다.
또한, 본 발명은 하기 화학식 1a 또는 1b로 표시되는 화합물을 제공하다:
상기 식에서,
A, X, R1 내지 R10은 앞서 정의된 바와 같고;
R11 내지 R21은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, 치환 또는 비치환된 C6-C40 아릴아미노, 치환 또는 비치환된 C6-C40 디아릴아미노, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며;
L은 직접 결합, 치환 또는 비치환된 C6-C40의 아릴렌 또는 치환 또는 비치환된 핵원자수 6 내지 40의 헤테로아릴렌이다.
본 발명에 따른 유기발광 화합물을 유기 EL 소자의 인광 또는 형광 호스트 재료로 채택하는 경우, 종래의 발광물질에 비해 호스트에서 도판트로의 에너지 이동이 원활이 이루어질 수 있다. 따라서, 본 발명에 따른 유기 EL 소자는 발광효율, 휘도, 전력효율, 구동전압 및 수명 면에서 우수한 특성을 나타낼 수 있어 풀 칼라 디스플레이 패널 등에 효과적으로 적용될 수 있다.
본 발명은 인광 호스트로서의 특성을 충분히 발휘하지 못하는 트리페닐렌과 같은 정공(hole) 제공 화합물 모이어티(moiety)를, 링커(L)를 통하거나 직접적인 결합을 통해 전자 제공능이 우수한 펜아진(phenazine) 계열의 화합물 모이어티(moiety)에 연결하여 충분히 높은 삼중항 에너지 레벨을 달성하는 화학식 1의 유기발광 화합물을 포함함으로써 인광특성을 개선함과 동시에 전자(electron) 및/또는 정공(hole) 수송 능력, 발광효율, 구동전압, 수명 특성 등에서 개선된 유기 EL 소자를 제공한다.
본 발명의 유기 EL 소자에 있어서, 화학식 1의 화합물은, X가 N이고; A가 치환 또는 비치환된, 핵원자수 6 내지 40의, 모노사이클릭 (monocyclic) 또는 축합 폴리사이클릭(fused polycyclic) 헤테로환(heterocycle)을 의미하되, 적어도 X-함유 고리는 핵원자수 6 내지 8의 방향족 고리인 화합물이다.
R1 내지 R10은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, (치환 또는 비치환된 C6-C40 아릴)C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며, R5 및 R6은 연결되어 축합고리를 형성할 수 있다.
R1 내지 R10의 알킬, 알케닐, 알키닐, 아릴, 헤테로아릴, 아릴옥시, 알킬옥시, 아릴알킬, 사이클로알킬 및 헤테로사이클로알킬은 각각 독립적으로 중수소, 할로겐, 아미노, 니트릴, 니트로, C1-C40 알킬, C2-C40 알케닐, C1-C40 알콕시, C3-C40 사이클로알킬, 핵원자수 3 내지 40의 헤테로사이클로알킬, C6-C40 아릴 및 핵원자수 5 내지 40의 헤테로아릴로 구성된 군으로부터 선택된 1 이상의 치환기로 치환될 수 있다.
본 발명의 화학식 1의 대표적인 화합물은 하기 화학식 1a 또는 1b의 화합물일 수 있다:
<화학식 1a>
<화학식 1b>
상기 식에서,
A, X, R1 내지 R10은 앞서 정의된 바와 같고;
R11 내지 R21은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, 치환 또는 비치환된 C6-C40 아릴아미노, 치환 또는 비치환된 C6-C40 디아릴아미노, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며;
L은 직접 결합, 치환 또는 비치환된 C6-C40의 아릴렌 또는 치환 또는 비치환된 핵원자수 6 내지 40의 헤테로아릴렌이며, 예를 들면 페닐렌, 바이페닐렌, 터페닐렌, 나프틸렌, 안트라세닐렌, 페난트릴렌, 피레닐렌, 플루오레닐렌, 카바조릴렌, N-카바졸페닐렌, 퀴놀리닐렌, 이소퀴놀리닐렌 등일 수 있다.
상기 링커 L의 아릴렌 및 헤테로아릴렌은 각각 독립적으로 중수소, C1-C40 알킬, C3-C40 사이클로알킬, C2-C40 알케닐, C1-C40 알콕시, C1-C40 알킬아미노, C6-C40 아릴 및 핵원자수 5 내지 40의 헤테로아릴로 구성된 군으로부터 선택되는 1 이상의 치환기로 치환될 수 있으며, 이러한 치환기는 인접하는 기와 스피로 결합을 이루거나 핵원자수 6 내지 40의 지방족, 방향족, 헤테로지방족 또는 헤테로방향족의 축합 고리를 형성할 수 있다.
또한, 상기 링커 L의 치환기인, 알킬, 사이클로알킬, 알케닐, 알콕시,알킬아미노, 아릴 및 헤테로아릴은 각각 독립적으로 중수소, 할로겐, 아미노, 니트릴, 니트로, C1-C40 알킬, C2-C40 알케닐, C1-C40 알콕시, C3-C40 사이클로알킬, 핵원자수 3 내지 40의 헤테로사이클로알킬, C6-C40 아릴 및 핵원자수 5 내지 40의 헤테로아릴로 구성된 군으로부터 선택된 1 이상의 치환기로 추가적으로 치환될 수 있다.
비제한적인 예로, 상기 링커 L은 하기 화학식 2의 구조식으로 이루어진 군에서 선택되는 C6-C40 아릴 또는 핵원자수 6 내지 40의 헤테로아릴인 것이 바람직하다.
상기 식에서,
k, m 및 n은 각각 독립적으로 1 내지 3 범위의 정수이고;
복수의 Q1은 서로 같거나 상이하며, 복수의 Q2는 서로 같거나 상이하며, 복수의 Q3는 서로 같거나 상이하며;
Q1, Q2 및 Q3는 서로 같거나 상이하고, 각각 독립적으로 수소; 중수소; 치환 또는 비치환된 C1-C40 알킬; 치환 또는 비치환된 C3-C40 사이클로알킬; 치환 또는 비치환된 C2-C40 알케닐; 치환 또는 비치환된 C1-C40 알콕시; 치환 또는 비치환된 C1-C40 알킬아미노; 치환 또는 비치환된 C6-C40 아릴; 또는 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴이며 이들 치환기는 인접하는 기와 핵원자수 6 내지 40의 지방족, 방향족, 헤테로지방족 또는 헤테로방향족의 축합 고리를 형성할 수 있다.
상기 알킬, 사이클로알킬, 알케닐, 알콕시, 알킬아미노, 아릴 및 헤테로아릴은 각각 독립적으로 중소수, 할로겐, 아미노, 니트릴, 니트로, C1-C40 알킬, C2-C40 알케닐, C1-C40 알콕시, C3-C40 사이클로알킬, C3-C40 헤테로사이클로알킬, C6-C40 아릴 및 핵원자수 5 내지 40의 헤테로아릴기로 이루어진 군에서 선택되는 하나 이상의 치환기로 치환될 수도 있다.
하기 화학식들은 본 발명의 화학식 1의 화합물의 대표적인 예들이나, 본 발명의 화합물이 하기 예시된 것들에 한정되는 것은 아니다.
본 발명에서 사용된 “비치환된 헤테로환(heterocycle)”은 핵원자수 6 내지 40의 방향족 또는 비-방향족 고리를 의미하며, 고리 중 하나 이상의 탄소, 바람직하게는 1 내지 3개의 탄소가 N, O 또는 S와 같은 헤테로원자로 치환된다. 헤테로환의 비-제한적인 예로는 3-1H-벤즈이미다졸-2-온, 2-테트라히드로퓨라닐, 2-테트라히드로티오페닐, 2-모르폴리닐, 3-모르폴리닐, 1-피롤리디닐, 1-피페라지닐, 2-피페라지닐, 4-티아졸리디닐, 벤족사닐(benzoxanyl), 벤조피롤리디닐(benzopyrrolidinyl), 벤조피페리디닐(benzopiperidinyl), 벤조티아닐(benzothianyl) 등이 포함된다. 나아가, 본원에서 사용된 헤테로환은 하나 이상의 방향족 또는 비-방향족 고리와 축합된 것도 포함하는 것으로 해석한다. 헤테로환의 하나 이상의 수소 원자는 중수소; C1-C40 알킬; C3-C40 사이클로알킬; C2-C40 알케닐; C1-C40 알콕시; C1-C40 알킬아미노; C6-C40 아릴; 또는 핵원자수 5 내지 40의 헤테로아릴로 치환될 수 있으며, 상기 알킬, 사이클로알킬, 알케닐, 알콕시, 알킬아미노, 아릴 및 헤테로아릴은 각각 독립적으로 중수소, 할로겐, 아미노, 니트릴, 니트로, C1-C40 알킬, C2-C40 알케닐, C1-C40 알콕시, C3-C40 사이클로알킬, C3-C40 헤테로사이클로알킬, C6-C40 아릴 및 핵원자수 5 내지 40의 헤테로아릴기로 이루어진 군에서 선택되는 하나 이상의 치환기로 치환될 수도 있다.
“비치환된 헤테로사이클로알킬”은 핵원자수 3 내지 40의 비-방향족 부위를 의미하며, 고리 중 하나 이상의 탄소, 바람직하게는 1 내지 3개의 탄소가 N, O 또는 S와 같은 헤테로 원자로 치환된다. 이의 비-제한적인 예로는 모르폴린, 피페라진 등이 있다.
“비치환된 헤테로아릴”은 핵원자수 5 내지 40의 모노헤테로사이클릭 또는 폴리헤테로사이클릭 방향족 부위를 의미하며, 고리 중 하나 이상의 탄소, 바람직하게는 1 내지 3개의 탄소가 N, O 또는 S와 같은 헤테로원자로 치환된다. 2 이상의 고리가 서로 단순 부착(pendant)되거나 축합된(fused) 형태로 부착될 수 있고, 나아가 아릴기와의 축합된 형태도 포함하는 것으로 해석한다. 헤테로아릴의 예로는 피리딜, 피라지닐, 피리미디닐, 피리다지닐, 트리아지닐과 같은 6-원 모노사이클릭 고리; 페녹사티에닐(phenoxathienyl), 인돌리지닐(indolizinyl), 인돌릴(indolyl), 퓨리닐(purinyl), 퀴놀릴(quinolyl), 벤조티아졸(benzothiazole), 카바졸릴(carbazolyl)과 같은 폴리사이클릭 고리를 포함하고, 2-퓨라닐, N-이미다졸릴, 2-이속사졸릴, 2-피리디닐, 2-피리미디닐 등도 포함하는 것으로 해석한다.
본 발명의 화학식 1의 화합물은 일반적인 합성방법에 따라 합성될 수 있다 (Macromoluecules, 38: 1131~1140 (2005); Organic Letters, 7: 4843~4846 (2005); J.Med.Chem, 44: 594~601 (2001); Chem Mater, 16: 5387~5393 (2004) 등 참조). 본 발명의 화합물에 대한 상세한 합성 과정은 후술하는 합성예에서 구체적으로 기술하도록 한다.
본 발명에 따른 유기 EL 소자는, 양극(anode); 음극(cathode); 및 상기 양극과 음극 사이에 개재(介在)된 1층 이상의 유기층을 포함하며, 상기 1층 이상의 유기층 중 적어도 하나는 상기 화학식 1로 표시되는 화합물을 포함하는 것을 특징으로 한다.
상기 화학식 1의 화합물은 단독 또는 복수로 포함될 수 있다.
본 발명의 화학식 1의 화합물을 포함하는 유기층은 정공주입층, 정공수송층, 전자수송층 및 발광층 중 어느 하나 이상일 수 있다. 본 발명에서 발광층은 인광 도판트 재료 또는 형광 도판트 재료를 포함할 수 있다. 바람직하게는, 본 발명의 화학식 1의 화합물은 청색, 녹색, 및/또는 적색의 인광 호스트, 형광 호스트, 정공수송 물질, 정공주입 물질 및/또는 전자수송물질로서 유기 EL 소자에 포함될 수 있다. 보다 바람직하게는 본 발명의 화학식 1의 화합물은 인광 호스트로서 유기 EL 소자에 포함될 수 있다.
본 발명의 화합물은 높은 유리 전이 온도를 가지고 있어, 이러한 화합물을 유기 EL 소자의 유기층으로 사용할 경우 유기 EL 소자 내에서 결정화가 최소화되기 때문에 소자의 구동전압을 낮출 수 있고, 발광효율, 휘도, 열적 안정성, 및 수명 특성을 개선할 수 있다.
본 발명에 따른 유기 EL 소자 구조의 비제한적인 예를 들면, 기판, 양극, 정공 주입층, 정공 수송층, 발광층, 전자 수송층 및 음극이 순차적으로 적층된 것일 수 있으며, 이때 상기 발광층, 정공주입층, 정공수송층 및 전자수송층 중 하나 이상은 상기 화학식 1로 표시되는 화합물을 포함할 수 있다. 상기 전자 수송층 위에는 전자 주입층이 위치할 수도 있다.
또한, 본 발명에 따른 유기 EL 소자는 전술한 바와 같이 양극, 1층 이상의 유기층 및 음극이 순차적으로 적층된 구조뿐만 아니라, 전극과 유기층 계면에 절연층 또는 접착층이 삽입될 수도 있다.
본 발명의 유기 EL 소자에 있어서, 상기 화학식 1의 화합물을 포함하는 상기 유기층은 진공 증착이나 용액 도포에 의하여 형성될 수 있다. 상기 용액 도포의 예 로는 스핀 코팅, 딥코팅, 닥터 블레이딩, 잉크젯 프린팅 또는 열 전사법 등이 있으나, 이들에만 한정되지 않는다.
본 발명의 유기 EL 소자는, 유기층 중 1층 이상을 본 발명의 화학식 1로 표현된 화합물을 포함하도록 형성하는 것을 제외하고는, 당 기술 분야에 알려져 있는 재료 및 방법을 이용하여 유기층 및 전극을 형성할 수 있다.
예컨대, 기판으로는 실리콘 웨이퍼, 석영, 유리판, 금속판, 플라스틱 필름이나 시트 등이 사용될 수 있다.
양극 물질로는 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연산화물, 인듐산화물, 인듐 주석 산화물(ITO), 인듐 아연 산화물(IZO)과 같은 금속 산화물; ZnO:Al 또는 SnO2:Sb와 같은 금속과 산화물의 조합물; 폴리티오펜, 폴리(3-메틸티오펜), 폴리[3,4-(에틸렌-1,2-디옥시)티오펜](PEDT), 폴리피롤 및 폴리아닐린과 같은 전도성 고분자; 또는 카본블랙 등이 있으나, 이들에만 한정되는 것은 아니다.
음극 물질로는 마그네슘, 칼슘, 나트륨, 칼륨, 타이타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석 또는 납과 같은 금속 또는 이들의 합금; LiF/Al 또는 LiO2/Al과 같은 다층 구조 물질 등이 있으나, 이들에만 한정되는 것은 아니다.
정공 주입층, 정공 수송층 및 전자전달층 및 전자 주입층은 특별히 한정되는 것은 아니며, 당 업계에 알려진 통상의 물질이 사용될 수 있다.
이하 본 발명을 실시예를 통하여 상세히 설명하면 다음과 같다. 단, 하기 실시예는 본 발명을 예시하는 것일 뿐 본 발명이 하기 실시예에 의해 한정되는 것은 아니다.
<
합성예
1> 화합물
In
-4의 합성
<단계 1> 화합물 3의 합성
화합물 1(10g, 1eq, 0.034mol), 화합물 2 (4.14g, 1.1eq, 0.038mol)을 1L 플라스크에 넣고 1-Butanol 500 ㎖를 첨가한 후 진한 황산 1 ㎖를 첨가하여 12시간 동안 환류 교반하였다.
반응이 종결된 후 증류수 200 ㎖와 메틸렌클로라이드(MC) 300 ㎖로 세척 및 추출하였다. 용매를 제거한 후 생성된 고체를 컬럼 크로마토그래피로 정제하여 화합물 3(10.2g, 수율 82%)를 수득하였다.
GC-Mass (이론치: 359.22g/mol, 측정치: 359g/mol)
<단계 2> 화합물 4의 합성
상기 <단계 1>에서 합성한 화합물 3(10g, 1eq, 0.027mol) 500 ㎖를 플라스크에 넣고 THF 250 ㎖를 첨가한 후 반응기 온도를 -78℃로 냉각시켰다. 여기에 1.6M n-BuLi (21.3 ㎖, 1.2eq, 0.033mol)를 서서히 첨가한 다음 대략 1시간 동안 교반하였다.
반응 1시간 후에 Triisopropylborate (7.6 ㎖, 1.2eq, 0.033mol)를 첨가하고 반응기의 온도를 상온으로 상승시킨 후 약 12시간 교반하였다.
반응이 종결된 후 반응 용액에 1N HCl 100 ㎖를 첨가하고 30분간 교반한 다음 에틸아세테이트(EA) 300 ㎖와 증류수 200 ㎖로 세척 및 추출하였다. 용매를 제거한 후 생성된 고체를 n-Hexane 200 ㎖와 혼합 교반하였다. 생성된 고체를 필터 여과하여 화합물 4(7.7g, 수율 88%)를 수득하였다.
GC-Mass (이론치: 324.14g/mol, 측정치: 324g/mol)
<단계 3> 화합물
In
-4의 합성
화합물 5(6.9g, 1eq, 0.017mol) 및 상기 <단계 2>에서 합성한 화합물 4(7g, 1.2eq, 0.021mol)를 플라스크에 넣고 Pd(PPh3)4 (0.39g, 0.02eq, 0.0003mol)를 첨가하였다. Toluene 250 ㎖ 및 2M K2CO3를 첨가한 다음 5시간 동안 환류 교반하였 다.
반응이 종결된 후 MC 500 ㎖와 증류수 200 ㎖로 세척 및 추출한 다음, 용매를 제거한 후 생성된 고체를 컬럼 크로마토그래피로 정제하여 원하는 표제 화합물 In-4(7.4g, 수율 75%)를 수득하였다.
GC-Mass (이론치: 582.69g/mol, 측정치: 582g/mol)
<
합성예
2> 화합물
In
-7의 합성
<단계 1> 화합물 2-3의 합성
화합물 2-1(10g, 1eq, 0.034mol) 및 화합물 2-2(4.14g, 1.1eq, 0.038mol)을 1L 플라스크에 넣고 아세트산 500 ㎖를 첨가한 다음 12시간 동안 환류 교반하였다.
반응이 종결된 후 증류수 1L를 첨가한 다음 생성된 고체를 여과하여 MC에 모두 녹인 후 증류수 200 ㎖로 세척하였다. 용매를 제거한 다음 생성된 고체를 컬럼 크로마토그래피로 정제하여 화합물 2-3(10g, 수율 80%)를 수득하였다.
GC-Mass (이론치: 361.23, 측정치: 361)
<단계 2> 화합물 2-4의 합성
상기 <단계 1>에서 합성한 화합물 2-3(10g, 1eq, 0.027mol)을 500 ㎖ 플라스크에 넣고 여기에 THF 250 ㎖를 첨가하였다. 반응기 온도를 -78℃로 냉각시킨 후 여기에 1.6M n-BuLi (21.3 ㎖, 1.2eq, 0.033mol)를 서서히 첨가하고 대략 1시간 동안 교반하였다.
반응 1시간 후, 반응기에 Triisopropylborate(7.6 ㎖, 1.2eq, 0.033mol)를 첨가하고 반응기의 온도를 상온으로 상승시킨 후 약 12시간 동안 교반하였다.
반응이 종결된 후 반응 용액에 1N HCl 100 ㎖를 첨가하고 30분간 교반하였다. EA 300 ㎖와 증류수 200 ㎖로 세척 및 추출한 다음, 용매를 제거하여 얻어진 고체를 n-Hexane 200 ㎖와 혼합 교반하였다. 생성된 고체를 필터 여과하여 화합물 2-4(7.6g, 수율 87%)를 수득하였다.
GC-Mass (이론치: 326.16g/mol, 측정치: 326g/mol)
<단계 3> 화합물
In
-7의 합성
화합물 2-5(6.9g, 1eq, 0.017mol) 및 상기 <단계 2>에서 합성한 화합물 2-4(7g, 1.2eq, 0.021mol)를 플라스크에 넣고 Pd(PPh3)4 (0.39g, 0.02eq, 0.0003mol) 를 첨가하였다. Toluene 250 ㎖ 및 2M K2CO3를 첨가한 다음 5시간 동안 환류 교반하였다.
반응이 종결된 후 MC 500 ㎖와 증류수 200 ㎖로 세척 및 추출한 다음, 용매를 제거한 후 생성된 고체를 컬럼 크로마토그래피로 정제하여 원하는 표제 화합물 In-4 (7.9g, 수율 80.1%)를 수득하였다.
GC-Mass (이론치: 584.71g/mol, 측정치: 584g/mol)
<
합성예
3> 화합물
In
-12의 합성
상기 합성예 1과 동일한 방법을 수행하되, <단계 3>에서 화합물 12-1 6.8 g 및 Pd(PPh3)4 0.4 g을 사용하여 표제 화합물 In-12(7.8g, 수율 75% 를 수득하였다.
GC-Mass (이론치: 582.69g/mol, 측정치: 582g/mol)
<
합성예
4> 화합물
In
-14의 합성
상기 합성예 2와 동일한 방법을 수행하되, <단계 3>에서 화합물 14-2(7.2g, 1eq, 0.018mol), 화합물 2-4(7.5g, 1.2eq, 0.022mol) 및 Pd(PPh3)4 (0.41g, 0.02eq, 0.0003mol)를 사용하여 표제 화합물 In-14(8.4g, 수율 82.6%)를 수득하였다.
GC-Mass (이론치: 584.71g/mol, 측정치: 584g/mol)
<
합성예
5> 화합물
In
-25의 합성
상기 합성예 1과 동일한 방법을 수행하되, <단계 3>에서 화합물 25-2(6g, 0.0112mol, 1eq), 화합물 4(4.35g, 0.0134mol, 1.2eq) 및 Pd(PPh3)4 (0.38g, 0.0003mol, 0.03eq)를 사용하여 표제 화합물 In-25(9.7g, 수율 85.4%)를 수득하였다.
GC-Mass (이론치: 734.88g/mol, 측정치: 734g/mol)
<
합성예
6> 화합물
In
-28의 합성
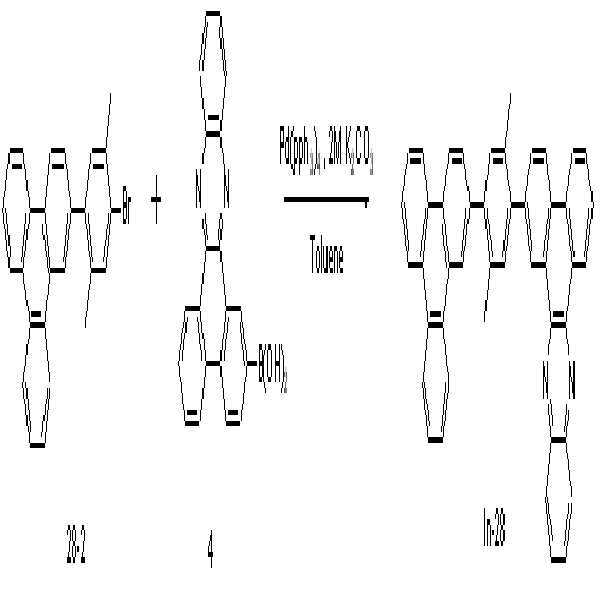
상기 합성예 1과 동일한 방법을 수행하되, <단계 3>에서 화합물 28-2(4.5g, 0.0109mol, 1eq), 화합물 4(4.23g, 0.013mol, 1.2eq) 및 Pd(PPh3)4 (0.35g, 0.00029mol, 0.03eq)를 사용하여 표제 화합물 In-28(8.2g, 수율 81.3%)을 수득하였다.
GC-Mass (이론치: 610.74g/mol, 측정치: 610g/mol)
<
합성예
7> 화합물
In
-31의 합성
상기 합성예 2와 동일한 방법을 수행하되, <단계 3>에서 화합물 28-2(4.5g, 0.0109 mol, 1eq), 화합물 2-4(4.21g, 0.013 mol, 1.2eq) 및 Pd(PPh3)4 (0.35g, 0.00029 mol, 0.03eq)를 사용하여 표제 화합물 In-31(7.9g, 수율 80.3%)을 수득하였다.
GC-Mass (이론치: 610.74g/mol, 측정치: 610g/mol)
<
합성예
8> 화합물
In
-36의 합성
상기 합성예 1과 동일한 방법을 수행하되, <단계 3>에서 화합물 36-2(4.8g, 0.0125mol, 1eq), 화합물 4(4.86g, 0.015mol, 1.2eq) 및 Pd(PPh3)4 (0.43g, 0.00375mol, 0.03eq)를 사용하여 표제 화합물 In-36(8.4g, 수율 87.1%)를 수득하였다.
GC-Mass (이론치: 583.68g/mol, 측정치: 583g/mol)
<
합성예
9> 화합물
In
-38의 합성
상기 합성예 2와 동일한 방법을 수행하되, <단계 3>에서 화합물 38-2(4.2g, 0.0109mol, 1eq), 화합물 2-4(4.56g, 0.015mol, 1.2eq) 및 Pd(PPh3)4 (0.41g, 0.0035mol, 0.03eq)를 사용하여 표제 화합물 In-38(7.9g, 수율 80.2%)를 수득하였다.
GC-Mass (이론치: 612.76g/mol, 측정치: 612g/mol)
[
실시예
1] 유기
EL
소자의 제조
ITO (Indium tin oxide)가 1500Å 두께로 박막 코팅된 유리 기판을 증류수 초음파로 세척하였다. 증류수 세척이 끝나면 이소프로필 알코올, 아세톤, 메탄올 등의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 이송시킨 다음 산소 플라즈마를 이용하여 상기 기판을 5분간 세정한 후 진공 층착기로 기판을 이송하였다.
이렇게 준비한 ITO (양극) 위에 DS-205(두산社)를 800Å 두께로 열 진공 증착하여 정공 주입층을 형성하고, 상기 정공 주입층 위에 정공 이송 물질인 a-NPB (N,N-di(naphthalene-1-yl)-N,N-diphenylbenzidine)을 150Å 두께로 진공 증착하였 다.
그 위에 상기 합성예 1에서 제조된 화합물 Inv-4 및 Ir(ppy)3를 300Å 두께로 진공 증착하여 발광층을 형성하고, 상기 발광층 위에 정공저지층 물질인 BCP를 200Å 두께로 형성한 다음 전자 수송 물질인 Alq3을 250Å 두께로 진공 증착하였다. 이 후, 전자 주입 물질인 LiF를 10Å 두께로 증착하고, 알루미늄 (음극)을 2000Å 두께로 진공 증착하여 하기 표 1과 같은 구조의 유기 EL 소자를 제작하였다.
[
실시예
2~8] 유기
EL
소자의 제조
발광층 형성시 합성예 1에서 제조된 화합물 In-4 대신 합성예 2-9에서 제조된 화합물을 사용한 것을 제외하고는, 실시예 1과 동일한 방법으로 유기 EL 소자를 제작하였다.
[
비교예
1] 유기
EL
소자의 제조
발광층 형성시 상기 합성예에서 제조된 화합물 대신 녹색 인광 호스트로 주로 사용되는 호스트인 CBP를 사용한 것을 제외하고는, 실시예 1과 동일한 방법으로 유기 EL 소자를 제작하였다.
| 정공주입층 (HIL) |
정공수송층 (HTL) |
발광층 (EML) |
정공저지층 (HBL) |
전자수송층 (ETL) |
전자주입층 (EIL) |
음극 |
|
| 실시예 1-9 | DS-205 | a-NPB | Inv 4, 7, 12, 14, 25, 28, 31, 36, 또는38 + Ir(ppy)3 | BCP | Alq3 | LiF | Al |
| 비교예 1 | DS-205 | a-NPB | CBP + Ir(ppy)3 | BCP | Alq3 | LiF | Al |
[
평가예
]
실시예 1-9 및 비교예 1에서 제작된 각각의 유기 EL 소자에 대하여 전류밀도 10 mA/㎠에서 측정된 발광 효율과, T=97 (9000nit)까지 측정된 시간(가속 수명)을 하기 표 2에 나타내었다.
| T=97 % / hr | 전압 (V) | 발광효율 (cd/A) | |
| In-4 | 104 | 6.01 | 60.2 |
| In-7 | 69 | 5.99 | 59.8 |
| In-12 | 107 | 6.2 | 66.9 |
| In-14 | 150 | 5.7 | 72.9 |
| In-25 | 96 | 5.73 | 54.2 |
| In-28 | 89 | 5.61 | 55.4 |
| In-31 | 109 | 5.9 | 63.7 |
| In-36 | 120 | 5.95 | 73.2 |
| In-38 | 115 | 6.04 | 60.1 |
| CBP | 78 | 6.22 | 44.79 |
상기 표 2를 살펴보면, 호스트 물질로서 본 발명에 따른 화합물을 사용한 유기 EL 소자는 종래 CBP를 사용한 유기 EL 소자보다 전압 및 효율 면에서 월등히 우수하며 특히 수명이 개선된 것을 확인할 수 있다.
이상을 통해 본 발명의 바람직한 실시예에 대하여 설명하였지만, 본 발명은 이에 한정되는 것이 아니고 특허청구범위와 발명의 상세한 설명의 범위 안에서 여러 가지로 변형하여 실시하는 것이 가능하고 이 또한 본 발명의 범위에 속하는 것은 당연하다.
Claims (5)
- 양극; 음극; 및 상기 양극과 음극 사이에 개재(介在)된 하나 이상의 유기층을 포함하는 유기 전계 발광 소자로서, 상기 유기층 중 적어도 하나는 하기 화학식 1a 또는 화학식 1b의 화합물을 포함하는 것을 특징으로 하는 유기 전계 발광 소자:<화학식 1a><화학식 1b>상기 식에서,X는 N이고;A는 치환 또는 비치환된, 핵원자수 6 내지 40의, 모노사이클릭 (monocyclic) 또는 축합 폴리사이클릭(fused polycyclic) 헤테로환(heterocycle)을 의미하되, 적어도 X-함유 고리는 핵원자수 6 내지 8의 방향족 고리이며;R1 내지 R10은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며, R5 및 R6은 연결되어 축합고리를 형성할 수 있으며,R11 내지 R21은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, 치환 또는 비치환된 C6-C40 아릴아미노, 치환 또는 비치환된 C6-C40 디아릴아미노, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며;L은 직접 결합, 치환 또는 비치환된 C6-C40의 아릴렌 또는 치환 또는 비치환된 핵원자수 6 내지 40의 헤테로아릴렌이다.
- 제 1 항에 있어서,상기 유기층은 발광층, 전자수송층, 정공 주입층 및 정공 수송층으로 구성된 군으로부터 선택되는 것을 특징으로 하는 유기 전계발광 소자.
- 제 1 항에 있어서,상기 화합물은 인광 호스트 물질 또는 형광 호스트 물질인 것을 특징으로 하는 유기 전계발광 소자.
- 하기 화학식 1a 또는 1b의 화합물:<화학식 1a><화학식 1b>상기 식에서,X는 N이고;A는 치환 또는 비치환된, 핵원자수 6 내지 40의, 모노사이클릭 (monocyclic) 또는 축합 폴리사이클릭(fused polycyclic) 헤테로환(heterocycle)을 의미하되, 적어도 X-함유 고리는 핵원자수 6 내지 8의 방향족 고리이며;R1 내지 R10은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며, R5 및 R6은 연결되어 축합고리를 형성할 수 있으며;R11 내지 R21은 각각 독립적으로 수소, 중수소, 치환 또는 비치환된 C1-C40 알킬, 치환 또는 비치환된 C2-C40 알케닐, 치환 또는 비치환된 C2-C40 알키닐, 치환 또는 비치환된 C6-C40 아릴, 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴, 치환 또는 비치환된 C6-C40 아릴옥시, 치환 또는 비치환된 C1-C40 알킬옥시, 치환 또는 비치환된 C6-C40 아릴아미노, 치환 또는 비치환된 C6-C40 디아릴아미노, (치환 또는 비치환된 C6-C40 아릴) C1-C40 알킬, 치환 또는 비치환된 C3-C40 사이클로알킬 또는 치환 또는 비치환된 핵원자수 3 내지 40의 헤테로사이클로알킬이며;L은 직접 결합, 치환 또는 비치환된 C6-C40의 아릴렌 또는 치환 또는 비치환된 핵원자수 6 내지 40의 헤테로아릴렌이다.
- 제 4 항에 있어서,상기 L은 하기 화학식 2의 구조식으로 이루어진 군에서 선택되는 것을 특징으로 하는 화합물:<화학식 2>상기 식에서,k, m 및 n은 각각 독립적으로 1 내지 3 범위의 정수이고;복수의 Q1은 서로 같거나 상이하며, 복수의 Q2는 서로 같거나 상이하며, 복수의 Q3는 서로 같거나 상이하며;Q1, Q2 및 Q3는 서로 같거나 상이하고, 각각 독립적으로 수소; 중수소; 치환 또는 비치환된 C1-C40 알킬; 치환 또는 비치환된 C3-C40 사이클로알킬; 치환 또는 비치환된 C2-C40 알케닐; 치환 또는 비치환된 C1-C40 알콕시; 치환 또는 비치환된 C1-C40 알킬아미노; 치환 또는 비치환된 C6-C40 아릴; 또는 치환 또는 비치환된 핵원자수 5 내지 40의 헤테로아릴이며 이들 치환기는 인접하는 기와 핵원자수 6 내지 40의 지방족, 방향족, 헤테로지방족 또는 헤테로방향족의 축합 고리를 형성할 수 있다.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020090134613A KR101290011B1 (ko) | 2009-12-30 | 2009-12-30 | 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 |
| PCT/KR2010/009477 WO2011081431A2 (ko) | 2009-12-30 | 2010-12-29 | 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020090134613A KR101290011B1 (ko) | 2009-12-30 | 2009-12-30 | 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20110077930A KR20110077930A (ko) | 2011-07-07 |
| KR101290011B1 true KR101290011B1 (ko) | 2013-07-30 |
Family
ID=44227033
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020090134613A KR101290011B1 (ko) | 2009-12-30 | 2009-12-30 | 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR101290011B1 (ko) |
| WO (1) | WO2011081431A2 (ko) |
Families Citing this family (81)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8314101B2 (en) * | 2007-11-30 | 2012-11-20 | Semiconductor Energy Laboratory Co., Ltd. | Quinoxaline derivative, and light-emitting element, light-emitting device, and electronic device using quinoxaline derivative |
| JP5606861B2 (ja) * | 2010-09-30 | 2014-10-15 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子用材料、膜、発光層、有機電界発光素子、及び有機電界発光素子の製造方法 |
| KR102082373B1 (ko) * | 2011-08-31 | 2020-02-27 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 복소환 화합물, 발광 소자, 발광 장치, 전자 기기, 조명 장치 및 유기 화합물 |
| JP5614568B1 (ja) * | 2013-02-07 | 2014-10-29 | 保土谷化学工業株式会社 | ジアザトリフェニレン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| KR101897039B1 (ko) * | 2014-05-22 | 2018-09-10 | 제일모직 주식회사 | 유기 화합물, 조성물, 유기 광전자 소자 및 표시 장치 |
| US9929361B2 (en) | 2015-02-16 | 2018-03-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11056657B2 (en) | 2015-02-27 | 2021-07-06 | University Display Corporation | Organic electroluminescent materials and devices |
| US9859510B2 (en) | 2015-05-15 | 2018-01-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10418568B2 (en) | 2015-06-01 | 2019-09-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11127905B2 (en) | 2015-07-29 | 2021-09-21 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10361381B2 (en) | 2015-09-03 | 2019-07-23 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN111303056B (zh) * | 2015-09-30 | 2022-02-11 | 北京鼎材科技有限公司 | 一种吩嗪基团取代的稠环芳烃衍生物及其应用 |
| KR102633649B1 (ko) * | 2015-11-19 | 2024-04-17 | 솔루스첨단소재 주식회사 | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20170073245A (ko) * | 2015-12-18 | 2017-06-28 | 삼성에스디아이 주식회사 | 유기 화합물, 조성물, 유기 광전자 소자 및 표시 장치 |
| US20170229663A1 (en) | 2016-02-09 | 2017-08-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10236456B2 (en) | 2016-04-11 | 2019-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11482683B2 (en) | 2016-06-20 | 2022-10-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10672997B2 (en) | 2016-06-20 | 2020-06-02 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10862054B2 (en) | 2016-06-20 | 2020-12-08 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10608186B2 (en) | 2016-09-14 | 2020-03-31 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680187B2 (en) | 2016-09-23 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11196010B2 (en) | 2016-10-03 | 2021-12-07 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11011709B2 (en) | 2016-10-07 | 2021-05-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20180130956A1 (en) | 2016-11-09 | 2018-05-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10680188B2 (en) | 2016-11-11 | 2020-06-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11780865B2 (en) | 2017-01-09 | 2023-10-10 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10844085B2 (en) | 2017-03-29 | 2020-11-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US10944060B2 (en) | 2017-05-11 | 2021-03-09 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12098157B2 (en) | 2017-06-23 | 2024-09-24 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11228010B2 (en) | 2017-07-26 | 2022-01-18 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11744142B2 (en) | 2017-08-10 | 2023-08-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20190161504A1 (en) | 2017-11-28 | 2019-05-30 | University Of Southern California | Carbene compounds and organic electroluminescent devices |
| EP3492480B1 (en) | 2017-11-29 | 2021-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11937503B2 (en) | 2017-11-30 | 2024-03-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11542289B2 (en) | 2018-01-26 | 2023-01-03 | Universal Display Corporation | Organic electroluminescent materials and devices |
| CN108727398B (zh) * | 2018-06-28 | 2020-03-17 | 宁波卢米蓝新材料有限公司 | 一种稠环化合物及其制备方法和用途 |
| US20200075870A1 (en) | 2018-08-22 | 2020-03-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20210320267A1 (en) * | 2018-09-27 | 2021-10-14 | Semiconductor Energy Laboratory Co., Ltd. | Light-emitting device, light-emitting apparatus, light-emitting module, electronic apparatus, lighting apparatus, organometallic complex, light-emitting material, organic compound, and dinuclear complex |
| KR102005866B1 (ko) * | 2018-11-12 | 2019-07-31 | 삼성에스디아이 주식회사 | 조성물, 유기 광전자 소자 및 표시 장치 |
| US11737349B2 (en) | 2018-12-12 | 2023-08-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US11780829B2 (en) | 2019-01-30 | 2023-10-10 | The University Of Southern California | Organic electroluminescent materials and devices |
| US20200251664A1 (en) | 2019-02-01 | 2020-08-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US12082428B2 (en) | 2019-03-12 | 2024-09-03 | Universal Display Corporation | OLED with triplet emitter and excited state lifetime less than 200 ns |
| JP2020158491A (ja) | 2019-03-26 | 2020-10-01 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネセンス材料及びデバイス |
| CN111848590B (zh) * | 2019-07-24 | 2022-08-12 | 广州华睿光电材料有限公司 | 化合物、高聚物、混合物、组合物及有机电子器件 |
| US20210032278A1 (en) | 2019-07-30 | 2021-02-04 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP2021031490A (ja) | 2019-08-16 | 2021-03-01 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネセンス材料及びデバイス |
| US20210135130A1 (en) | 2019-11-04 | 2021-05-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| JP7488091B2 (ja) | 2019-11-14 | 2024-05-21 | ユニバーサル ディスプレイ コーポレイション | 有機エレクトロルミネセンス材料及びデバイス |
| US20210217969A1 (en) | 2020-01-06 | 2021-07-15 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220336759A1 (en) | 2020-01-28 | 2022-10-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP3937268A1 (en) | 2020-07-10 | 2022-01-12 | Universal Display Corporation | Plasmonic oleds and vertical dipole emitters |
| US20220158096A1 (en) | 2020-11-16 | 2022-05-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220162243A1 (en) | 2020-11-24 | 2022-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220165967A1 (en) | 2020-11-24 | 2022-05-26 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220271241A1 (en) | 2021-02-03 | 2022-08-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4059915A3 (en) | 2021-02-26 | 2022-12-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4060758A3 (en) | 2021-02-26 | 2023-03-29 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220298192A1 (en) | 2021-03-05 | 2022-09-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220298190A1 (en) | 2021-03-12 | 2022-09-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220298193A1 (en) | 2021-03-15 | 2022-09-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20220340607A1 (en) | 2021-04-05 | 2022-10-27 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4075531A1 (en) | 2021-04-13 | 2022-10-19 | Universal Display Corporation | Plasmonic oleds and vertical dipole emitters |
| US20220352478A1 (en) | 2021-04-14 | 2022-11-03 | Universal Display Corporation | Organic eletroluminescent materials and devices |
| US20220407020A1 (en) | 2021-04-23 | 2022-12-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230006149A1 (en) | 2021-04-23 | 2023-01-05 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230133787A1 (en) | 2021-06-08 | 2023-05-04 | University Of Southern California | Molecular Alignment of Homoleptic Iridium Phosphors |
| EP4151699A1 (en) | 2021-09-17 | 2023-03-22 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240343970A1 (en) | 2021-12-16 | 2024-10-17 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230292592A1 (en) | 2022-03-09 | 2023-09-14 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230337516A1 (en) | 2022-04-18 | 2023-10-19 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20230389421A1 (en) | 2022-05-24 | 2023-11-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| EP4293001A1 (en) | 2022-06-08 | 2023-12-20 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240016051A1 (en) | 2022-06-28 | 2024-01-11 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240107880A1 (en) | 2022-08-17 | 2024-03-28 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240188419A1 (en) | 2022-10-27 | 2024-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240196730A1 (en) | 2022-10-27 | 2024-06-13 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240188319A1 (en) | 2022-10-27 | 2024-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240180025A1 (en) | 2022-10-27 | 2024-05-30 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240188316A1 (en) | 2022-10-27 | 2024-06-06 | Universal Display Corporation | Organic electroluminescent materials and devices |
| US20240247017A1 (en) | 2022-12-14 | 2024-07-25 | Universal Display Corporation | Organic electroluminescent materials and devices |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003040873A (ja) * | 2001-07-25 | 2003-02-13 | Idemitsu Kosan Co Ltd | 新規キノキサリン誘導体及びそれを利用した有機エレクトロルミネッセンス素子 |
| JP2007099766A (ja) * | 2005-09-12 | 2007-04-19 | Semiconductor Energy Lab Co Ltd | キノキサリン誘導体、およびキノキサリン誘導体を用いた発光素子、発光装置、電子機器 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101625235B1 (ko) * | 2007-09-20 | 2016-05-27 | 바스프 에스이 | 전계발광 소자 |
| US8314101B2 (en) * | 2007-11-30 | 2012-11-20 | Semiconductor Energy Laboratory Co., Ltd. | Quinoxaline derivative, and light-emitting element, light-emitting device, and electronic device using quinoxaline derivative |
-
2009
- 2009-12-30 KR KR1020090134613A patent/KR101290011B1/ko active IP Right Grant
-
2010
- 2010-12-29 WO PCT/KR2010/009477 patent/WO2011081431A2/ko active Application Filing
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003040873A (ja) * | 2001-07-25 | 2003-02-13 | Idemitsu Kosan Co Ltd | 新規キノキサリン誘導体及びそれを利用した有機エレクトロルミネッセンス素子 |
| JP2007099766A (ja) * | 2005-09-12 | 2007-04-19 | Semiconductor Energy Lab Co Ltd | キノキサリン誘導体、およびキノキサリン誘導体を用いた発光素子、発光装置、電子機器 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2011081431A2 (ko) | 2011-07-07 |
| KR20110077930A (ko) | 2011-07-07 |
| WO2011081431A3 (ko) | 2011-12-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101290011B1 (ko) | 유기발광 화합물 및 이를 포함한 유기 전계 발광 소자 | |
| KR101412437B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| EP2937347B1 (en) | Novel compound and organic electronic element using same | |
| KR102192691B1 (ko) | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 | |
| KR101657015B1 (ko) | 유기 전자 소자 재료 및 이를 포함하는 유기 전자 소자 | |
| KR20100119077A (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| KR101628438B1 (ko) | 함질소 헤테로환 화합물 및 이를 포함하는 유기 전자 소자 | |
| KR20170038748A (ko) | 스피로형 화합물 및 이를 포함하는 유기 발광 소자 | |
| KR101560061B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| EP3345891B1 (en) | Amine compound and organic light-emitting device comprising same | |
| KR101597865B1 (ko) | 신규한 화합물 및 이를 이용한 유기 전자 소자 | |
| KR20170057850A (ko) | 화합물 및 이를 포함하는 유기 전자 소자 | |
| KR101634853B1 (ko) | 유기 화합물 및 이를 포함하는 유기 전계 발광 소자 | |
| KR101380008B1 (ko) | 신규한 안트라센 유도체 및 이를 이용한 유기 전자 소자 | |
| KR20180023626A (ko) | 유기 광전자 소자용 화합물, 유기 광전자 소자 및 표시 장치 | |
| KR20190118917A (ko) | 화합물 및 이를 포함하는 유기 발광 소자 | |
| KR101584855B1 (ko) | 함질소 헤테로환 화합물 및 이를 포함한 유기 전자소자 | |
| KR101926022B1 (ko) | 유기 화합물, 유기 광전자 소자 및 표시 장치 | |
| KR101350524B1 (ko) | 신규한 안트라센 유도체 및 이를 이용한 유기 전자 소자 | |
| KR20190035070A (ko) | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 | |
| KR102221403B1 (ko) | 화합물 및 이를 포함하는 유기 발광 소자 | |
| KR20130098260A (ko) | 신규한 안트라센 유도체 및 이를 이용한 유기 전자 소자 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20160627 Year of fee payment: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20170719 Year of fee payment: 5 |